题目内容
1.氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用.(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2 (g)=4NO (g)+6H2O (L)△H1
②4NH3(g)+6NO(g)=5N2 (g)+6H2O (L)△H2
则反应 4NH3(g)+3O2(g)=2N2 (g)+6H2O (L)△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol N2 在一定条件下合成氮,平衡时仅改变温度测得的数据如下表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则 T1、<T2(填“>”、“<”或“=”)
②T2K下,经过10min达到化学平衡状态,则o~10min内H2的平均速率v(H2)=0.1mol•L-1•min-1.
③下列图象分别代表焓变(△H),混合气体平均相对分子质量($\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态是BC.

(3)电化学降解治理水中硝酸盐污染,在酸性条件下,电化学降解NO3-的原理如图1,阴极反应式为2NO3-+12H++10e-=N2↑+6H2O.

(4)通过控制溶液的pH对工业废水中的金属离子进行分离.图2是某些金属氢氧化物在不同浓度和pH的沉淀--溶解图象,图中直线上的点表示平衡状态.当溶液中的离子浓度小于1×10-5mol•L-1时,认为该离子沉淀完全.
由图可知Cu(OH)2的浓度积的值为1×10-21.8.
分析 (1)由①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×$\frac{1}{5}$得到4NH3(g)+3O2(g)=2N2(g)+6H2O(l);
(2)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
结合v=$\frac{△c}{△t}$计算;
③焓变(△H)始终不变,混合气体平均相对分子质量($\overline{M}$)为变量、N2体积分数φ(N2)为变量,气体密度(ρ)始终不变;
(3)由图可知,硝酸根离子发生还有反应生成氮气,为阴极反应;
(4)当PH=5.6时,c(Cu2+)=1×10-5mol•L-1,再根据Ksp表达式求算.
解答 解:(1)由①4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H2
结合盖斯定律可知,(①×3+②×2)×$\frac{1}{5}$得到4NH3(g)+3O2(g)=2N2(g)+6H2O(l),则△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$,
故答案为:$\frac{3△{H}_{1}+2△{H}_{2}}{5}$;
(2)破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量,则合成氨的反应为放热反应,
①由表格数据可知,T1对应的氨气平衡时物质的量大,则T1的温度低,则T1<T2,故答案为:<;
②T2K下,经过10min达到化学平衡状态,则
N2+3 H2?2NH3,
开始 4 9 0
转化 1 3 2
平衡 3 6 2
v(H2)=$\frac{△c}{△t}$=$\frac{\frac{3mol}{3L}}{10min}$=0.1mol•L-1•min-1,
故答案为:0.1mol•L-1•min-1;
③焓变(△H)始终不变,混合气体平均相对分子质量($\overline{M}$)为变量、N2体积分数φ(N2)为变量,气体密度(ρ)始终不变,随反应进行,气体的物质的量减小,则$\overline{M}$随时间增大而增大,直到达到平衡状态不变;N2体积分数逐渐减小,到达到平衡状态不变,由图可知,正确且能表明该可逆反应达到平衡状态的为BC,
故答案为:BC;
(3)由图可知,硝酸根离子发生还有反应生成氮气,则Ag-Pt电极为阴极,Pt电极为阳极,则A为电池的正极,阴极上硝酸根获得电子,与通过质子交换膜的氢离子作用生成氮气与水,阴极电极反应式为:2NO3-+12H++10e-=N2↑+6H2O,
故答案为:2NO3-+12H++10e-=N2↑+6H2O;
(4)由图象可知,当PH=5.6时,c(Cu2+)=1×10-5mol•L-1,Ksp=c(Cu2+)•c2(OH-)=1×10-5×(1×10-8.4)2 =1×10-21.8,故答案为:1×10-21.8.
点评 本题考查较综合,为高考常见题型,涉及化学平衡图象、平衡计算、盖斯定律的应用及计算、电化学原理及计算等,综合性较强,侧重化学反应原理中高频考点的考查,题目难度中等.

 字词句段篇系列答案
字词句段篇系列答案| A. | 甲烷是天然气的主要成分,能发生取代反应,但不能发生氧化反应 | |
| B. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| C. | 只用水无法鉴别苯、乙酸和四氯化碳 | |
| D. | 植物油不能用于萃取溴水中的溴 |
| A. | 78g苯中含有的碳碳双键的数目为3NA | |
| B. | 16g由Cu2S和CuO组成的混合物中含有的阳离子数为0.2NA | |
| C. | 将1molH2与1molI2充入一密闭容器中充分反应后,转移的电子数为2NA | |
| D. | 1mo1Fe与足量的浓硫酸共热反应,生成SO2的分子数为NA |
(1)已知反应CO(g)+2H2(g)═CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如表:
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:
CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1<0,
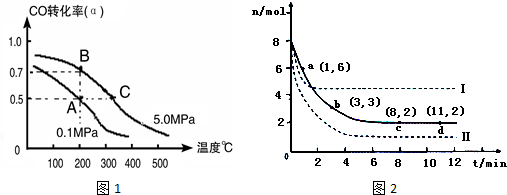
CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.

①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)表中元素③的原子结构示意图
 ;元素⑨形成的氢化物的电子式
;元素⑨形成的氢化物的电子式 .
.(3)表中元素④、⑨形成的氢化物的稳定性顺序为HF>HCl(填化学式).
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为HClO4>H2SO4(填化学式).
(5)表中元素③、④、⑥、⑦的原子半径大小为Na>Mg>O>F(填元素符号).

下列说法正确的是( )
| A. | 溶解烧渣选用足量酸,可以从常见的强酸中选择任意一种,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,只需要缓慢加热至溶液出现少量晶体,停止加热利用余热蒸干即可 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
| A. | 非金属原子间以共价键结合的物质一定是共价化合物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 凡是能电离出离子的化合物一定是离子化合物 | |
| D. | 凡是含有离子键的化合物一定是离子化合物 |
 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构为:有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构为:有关该化合物的下列说法不正确的是( )| A. | 分子式为C13H20O | |
| B. | 该化合物可发生聚合反应 | |
| C. | 1 mol该化合物完全燃烧消耗19 mol O2 | |
| D. | 1mol该化合物与足量H2加成,最多消耗H23mol |