题目内容
12.下列各组分子中,都属于含极性键的非极性分子的是( )| A. | CO2H2S | B. | NH3 HCl | C. | P4 CCl4 | D. | C2H4 CH4 |
分析 不同非金属元素之间形成极性键,结构对称、正负电荷的中心重合时为非极性分子,以此来解答.
解答 解:A.H2S含极性键,为V型结构,属于极性分子,故A不选;
B.NH3、HCl均为含极性键的极性分子,故B不选;
C.P4、CCl4均为正四面体结构,为非极性分子,但P4只含P-P非极性键,故C不选;
D.C2H4、CH4分别为平面结构、正四面体结构,均为非极性分子,且均含C-H极性键,故D选;
故选D.
点评 本题考查化学键及分子极性,为高频考点,把握化学键的类型及判断、分子结构为解答的关键,侧重分析与应用能力的考查,注意常见物质的结构,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列说法正确的是 ( )
| A. | 钠、镁、铝原子半径依次增大 | B. | NH3H2O HF 稳定性依次减弱 | ||
| C. | H3PO4H2SO4HClO4酸性依次增强 | D. | NaOH Mg(OH)2 Al(OH)3碱性依次增强 |
3.下列反应的离子方程式书写正确的是( )
| A. | 氯化钠与浓硫酸混合加热:H2SO4(浓)+2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$SO${\;}_{4}^{2-}$+2HCl↑ | |
| B. | 过量的硫化钠溶液与氯化铁溶液反应:2Fe3++S2-═2Fe2++S↓ | |
| C. | 碳酸氢铵溶液与足量NaOH溶液混合后加热:NH${\;}_{4}^{+}$+HCO${\;}_{3}^{-}$+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$CO${\;}_{3}^{2-}$+NH3↑+2H2O | |
| D. | 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
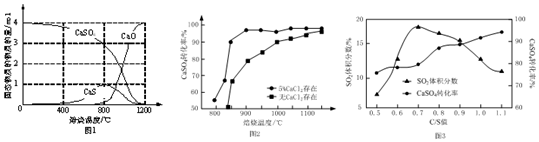
20.目前,我市电能的主要来源是火力发电. 下列关于火力发电过程中能量转化关系的描述,正确的是( )

| A. | 化学能转化成机械能在转化成电能 | |
| B. | 化学能转化成热能在转化成电能 | |
| C. | 化学能转化成机械能在转化成热能在到机械能 | |
| D. | 化学能转化成热能在转化成机械能在到电能 |
7.下列各组递变情况描述错误的是( )
| A. | H、Be、B 原子最外层电子数依次增多 | |
| B. | P、S、Cl 元素最高正化合价依次升高 | |
| C. | F2、Cl2、Br2、I2的熔点依次降低 | |
| D. | Li、Na、K、Rb的金属性依次增强 |
17.一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
| A. | 若增大压强,则物质Y的转化率减小 | |
| B. | 将容器体积变为5 L,Z的平衡浓度变为原来的2倍 | |
| C. | Y浓度变化表示的反应速率为0.0005 mol/(L•s ) | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
4.对于下列事实的解释错误的是( )
| A. | 在蔗糖中加入浓硫酸后出现发黑的现象,说明浓硫酸具有脱水性 | |
| B. | Na的金属活动性比Mg强,说明可用Na与MgCl2溶液反应制Mg | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸反应生成了致密的氧化物 | |
| D. | 向碘水中滴加CCl4,振荡静置后分层,下层呈紫红色,说明可用CCl4从碘水中萃取碘 |
 .
.