题目内容
3.下列反应的离子方程式书写正确的是( )| A. | 氯化钠与浓硫酸混合加热:H2SO4(浓)+2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$SO${\;}_{4}^{2-}$+2HCl↑ | |
| B. | 过量的硫化钠溶液与氯化铁溶液反应:2Fe3++S2-═2Fe2++S↓ | |
| C. | 碳酸氢铵溶液与足量NaOH溶液混合后加热:NH${\;}_{4}^{+}$+HCO${\;}_{3}^{-}$+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$CO${\;}_{3}^{2-}$+NH3↑+2H2O | |
| D. | 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
分析 A.该反应不是发生在溶液中的反应,不能书写离子方程式;
B.硫化钠过量,反应生成FeS沉淀;
C.氢氧化钠足量,铵根离子和碳酸氢根离子都完全反应;
D.二氧化硫少量,反应生成硫酸钙沉淀.
解答 解:A.氯化钠溶液和浓硫酸混合加热的反应:2NaCl+H2SO4(浓)═Na2SO4+2HCl↑,该反应无法书写离子方程式,故A错误;
B.过量的硫化钠溶液与氯化铁溶液,反应生成硫化亚铁沉淀,正确的离子方程式为:2Fe3++3S2-═2FeS↓+S↓,故B错误;
C.碳酸氢铵溶液与足量NaOH溶液混合后加热,反应生成碳酸钠、氨气和水,反应的离子方程式为2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$CO32-+NH3↑+2H2O,故C正确;
D.向次氯酸钙溶液中通入少量SO2,反应生成硫酸钙沉淀、次氯酸和氯化钠,正确的离子方程式为:Ca2++3ClO-+H2O+SO2═CaSO4↓+2HClO+Cl-,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
13.pH=3的盐酸和pH=11的氨水等体积混合,溶液中离子浓度关系正确的是( )
| A. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) | B. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | ||
| C. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
14.反应A(g)+3B(g)═2C(g)+2D(g),在四种不同的情况下的反应速率v,其中反应进行最快的是( )
| A. | v(A)=0.2mol•(L•s)-1 | B. | v(C)=0.5 mol•(L•s)-1 | ||
| C. | v(B)=0.6 mol•(L•s)-1 | D. | v(D)=0.3 mol•(L•s)-1 |
11.下列化合物中既易发生取代反应,也可发生加成反应,还能使KMnO4酸性溶液褪色的是( )
| A. | 甲苯 | B. | 乙醇 | C. | 甲烷 | D. | 苯 |
8.同温同压下,四个等体积的干燥圆底烧瓶中分别充满:①NH3 ②HCl(混有少量空气),③NO2,④NO2和O2(4:1)的混合气体,进行喷泉实验,经充分反应后,圆底瓶内溶液的物质的量浓度为(设溶质不扩散)( )
| A. | ①>②>③>④ | B. | ①=②=③=④ | C. | ①=②=③>④ | D. | ①>②>③=④ |
15.CO2 分子中σ键与π键数目比为( )
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 1:3 |
12.下列各组分子中,都属于含极性键的非极性分子的是( )
| A. | CO2H2S | B. | NH3 HCl | C. | P4 CCl4 | D. | C2H4 CH4 |
13.已知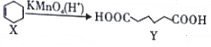 ,下列说法错误的是( )
,下列说法错误的是( )
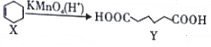 ,下列说法错误的是( )
,下列说法错误的是( )| A. | X分子中所有碳原子一定在同一平面上 | |
| B. | X与乙烯不属于同系物 | |
| C. | Y可发生取代反应、氧化反应 | |
| D. | Y的含有相同官能团的同分异构体有8种(不考虑立体异构) |
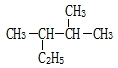 用系统命名法命名:2,3-二甲基丁烷
用系统命名法命名:2,3-二甲基丁烷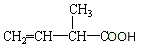 官能团的名称是碳碳双键、羧基
官能团的名称是碳碳双键、羧基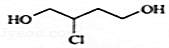 的分子式为C4H9O2Cl
的分子式为C4H9O2Cl