题目内容
10.如图是有关电化学的图示,完全正确的是( )| A. | 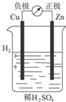 Cu-Zn原电池 | B. | 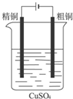 粗铜的精炼 | C. | 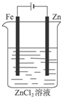 铁片镀锌 | D. | 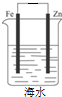 减缓铁腐蚀 |
分析 A.依据原电池原理分析,活泼金属做负极;
B.粗铜精炼,粗铜做阳极,精铜做阴极;
C.依据电镀原理,镀层金属做阳极,待镀金属做阴极;
D.作原电池的负极被腐蚀,作正极被保护.
解答 解:A.锌比铜活泼,应为负极,铜为正极,故A错误;
B.粗铜精炼,粗铜做阳极,精铜做阴极,故B错误;
C.镀件铁做阴极,锌做阳极进行电镀,故C错误;
D.Fe、Zn形成原电池时,Zn作原电池的负极被腐蚀,Fe作正极被保护,故D正确;
故选D.
点评 本题考查了原电池和电解池原理的分析判断,为高频考点,侧重于学生的分析能力的考查,注意把握电极反应和电极判断,题目难度中等.

练习册系列答案
相关题目
20.下列有关能量的说法正确的是( )
| A. | 原电池将化学能转变为电能 | |
| B. | 原电池将电能转变为化学能 | |
| C. | 中和反应放热说明中和反应前后能量不守恒 | |
| D. | 吸热反应中生成物的总能量低于反应物的总能量 |
18.在甲酸溶液中加入一定量的NaOH溶液,恰好完全反应,对于生成的溶液,下列判断一定正确的是( )
| A. | c(HCOO-)<c(Na+) | B. | c(HCOO-)>c(Na+) | C. | c(OH-)>c(HCOO-) | D. | c(OH-)<c(HCOO-) |
5.除去苯中少量苯酚的方法是( )
| A. | 加FeCl3溶液、分液 | B. | 加浓溴水、过滤 | ||
| C. | 加液溴反应后蒸馏 | D. | 加NaOH溶液、分液 |
15.下列反应中属于氧化还原反应的是( )
| A. | Ca2CO3+2HCl═CaCl2+H2O+CO2↑ | B. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2↑ | ||
| C. | Cu+4HNO3(稀)═Cu(NO3)2+2NO↑+2H2O | D. | NaCl+AgNO3═AgCl↓+NaNO3 |
19.酚酞的结构如图,则下列说法中正确的是( )


| A. | 分子式是C20H12O4 | B. | 能与NaOH稀溶液反应,溶液显红色 | ||
| C. | 能与溴水反应,溶液显红色 | D. | 与羧酸发生酯化反应 |
20.室温时,将浓度和体积分别为c1,V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A. | 当pH=7时,若V1=V2,则一定是c2>c1 | |
| B. | 在任何情况下都满足c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 若pH>7,则一定是c1V1>c2V2 | |
| D. | 若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |