题目内容
3.下列关于杂化轨道的叙述正确的是( )| A. | 杂化轨道的数目、形状和参与杂化的原子轨道数目、形状均相同 | |
| B. | 等性杂化轨道的形状、能量相等; NH3中N是等性杂化 | |
| C. | 各杂化轨道在空间应满足电子对互斥理论,以使排斥力最小 | |
| D. | sp3杂化轨道应由同原子里能量相同的s和p轨道杂化而得 |
分析 A.杂化轨道的数目与参与杂化的原子轨道数目相同,但形状不相同;
B.杂化后的杂化轨道至少存在两个不同的,说明是非等性杂化;
C.各杂化轨道在空间应满足电子对互斥理论,以使排斥力最小,使分子能量最低;
D.sp3杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道,杂化后的各轨道完全相同.
解答 解:A.杂化轨道的数目与参与杂化的原子轨道数目相同,但形状发生变化,所以形状不相同,故A错误;
B.杂化后的杂化轨道至少存在两个不同的,说明是非等性杂化,如如氨气分子中,N原子虽是sp3杂化,但杂化后的四个轨道不完全相同,是非等性杂化,故B错误;
C.各杂化轨道在空间应满足电子对互斥理论,以使排斥力最小,使分子能量最低,分子最稳定,故C正确;
D.sp3杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道,故D错误;
故选C.
点评 本题考查杂化轨道的有关知识,为高频考点,侧重考查学生理解、判断能力,明确杂化轨道形成原理是解本题关键,知道哪些轨道能形成杂化轨道,题目难度中等.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
20.对于100mL1mol/L盐酸与铁片的反应,采取下列措施:①升高温度;②改用300mL1mol/L盐酸;③改用100mL3mol/L盐酸;④用等量铁粉代替铁片;⑤改用98%的硫酸.其中能使反应速率加快的是( )
| A. | ①③④ | B. | ①②④ | C. | ①②③④ | D. | ①②③⑤ |
11.下列有关物质用途叙述不正确的是( )
| A. | 从环境保护角度,氟氯代烷不宜用作制冷剂 | |
| B. | 聚氯乙烯制品适宜用于直接盛装食物 | |
| C. | 苯、甲苯、二甲苯都是基本的有机化工原料 | |
| D. | 乙烯用作果实催熟剂 |
12.白磷有剧毒,白磷中毒可用硫酸铜溶液解毒,白磷与硫酸铜可以发生如下两个反应:
(1)2P+5CuSO4+8H2O═5Cu+2H3PO4+5H2SO4
(2)11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4
下列有关说法中错误的是( )
(1)2P+5CuSO4+8H2O═5Cu+2H3PO4+5H2SO4
(2)11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4
下列有关说法中错误的是( )
| A. | 上述两个反应中,水既不是氧化剂也不是还原剂 | |
| B. | 上述两个反应中,氧化产物都是H3PO4 | |
| C. | 反应(2)中,1mol CuSO4可氧化1/5molP | |
| D. | 上述两个反应中,氧化剂都只有硫酸铜 |
13.已知NH4CuSO3与足量的2mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成,②产生刺激性气味的气体,③溶液呈现蓝色,据此判断下列说法正确的是( )
| A. | 反应中硫酸做还原剂,有铜被还原 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 2mol NH4CuSO3完全反应转移6.02×1023个电子 | |
| D. | 刺激性气味的气体是氨气 |
 从海带中提取单质碘及碘的化合物间的转化关系如图所示:
从海带中提取单质碘及碘的化合物间的转化关系如图所示:
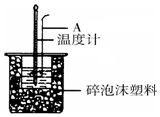 50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算反应热.
50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算反应热.