题目内容
9.Y元素的阳离子和X元素的阴离子具有与氩原子相同的电子层结构,下列叙述不正确的是( )| A. | Y的原子序数比X的大 | B. | Y的原子半径比X的大 | ||
| C. | Y原子的最外层电子数比X的大 | D. | Y元素的最高正价比X的大 |
分析 Y元素的阳离子和X元素的阴离子具有与氩原子相同的电子层结构,则三微粒核外电子数相同,X与氩同周期,Y在它们的下一周期,最外层电子数Y<X<Ar,结合元素周期律解答.
解答 解:A.Y元素的阳离子和X元素的阴离子具有与氩原子相同的电子层结构,则三微粒核外电子数相同,X与氩同周期,Y在它们的下一周期,三种粒子其原子序数关系应为:Y>Ar>X,故A正确;
B.Y元素形成阳离子,X元素形成阴离子,最外层电子数X>Y,Y在X的下一周期,原子半径Y>X,故B正确;
C.Y元素形成阳离子,X元素形成阴离子,最外层电子数X>Y,故C错误;
D.最外层电子数X>Y,则最高正价X>Y,故D错误.
故选CD.
点评 本题考查考生对核外电子排布式的理解能力,对金属、非金属、稀有气体元素原子电子层结构特点和得失电子能力理解,掌握元素原子结构与在周期表中所处位置、原子半径大小关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.用2mol/L的硝酸银溶液10mL,分别与相同体积的下列溶液恰好完全反应,则下列溶液中物质的量浓度最小的是( )
| A. | BaCl2 | B. | MgCl2 | C. | KCl | D. | FeCl3 |
4.配制0.1mol/L的NaOH溶液,下列操作会使实验结果偏低的是( )
| A. | 用滤纸称量NaOH固体 | B. | 移液前容量瓶内有水珠 | ||
| C. | 摇匀后,液面低于刻度线 | D. | 定容时,俯视刻度线 |
14.水溶液X中只可能含有K+、Mg2+、Al3+、AlO2-、SiO32-、SO32-、CO32-、SO42-中的若干种离子.某同学对该溶液X进行了如下实验:下列判断正确的是( )
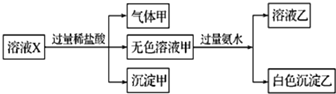

| A. | 气体甲一定是纯净物 | |
| B. | 沉淀甲是硅酸和硅酸镁的混合物 | |
| C. | K+、AlO2-和SiO32-一定存在于溶液X中 | |
| D. | 仅凭以上实验不能确定SO42-是否存在于溶液X中 |
18.分子式为C8H10的某有机物,它能使酸性高锰酸钾溶液褪色,但不能使溴水反应.符合条件的有机物的一氯代物的同分异构体有( )
| A. | 14 种 | B. | 16 种 | C. | 18 种 | D. | 19 种 |
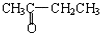 B.
B.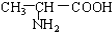 与
与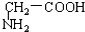
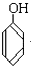 与
与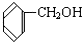 D.CH3CH2C≡CH与CH2═CH-CH═CH2E.
D.CH3CH2C≡CH与CH2═CH-CH═CH2E.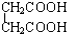 与
与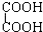 F.戊烯和环丙烯
F.戊烯和环丙烯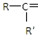 氧化成(R、R′
氧化成(R、R′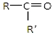 可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.
可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.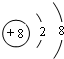 ;
;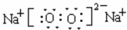 ;
;