题目内容
7.实验室制取下列物质的实验中未利用冷凝原理的是( )| A. | 乙酸乙酯 | B. | 乙酸丁酯 | C. | 溴乙烷 | D. | 乙烯 |
分析 实验室利用冷凝原理,因反应物易挥发,降低其利用率,则冷凝回流可充分利用反应物,以此来解答.
解答 解:A.乙酸、乙醇均易挥发,发生酯化反应时利用冷凝原理可充分利用反应物,故A不选;
B.乙酸易挥发,发生酯化反应时利用冷凝原理可充分利用反应物,故B不选;
C.利用乙烯与HBr发生加成反应制备,HBr需要冷凝回流增大利用率,故C不选;
D.浓硫酸与乙醇加热到170℃时发生消去反应制备乙烯,不需要冷凝原理,故D选;
故选D.
点评 本题考查有机物制备实验评价,为高频考点,把握有机物的官能团与性质、反应原理及实验装置为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
18.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4═2PbSO4↓+2H2O,根据此反应判断下列有关该电池的说法错误的是( )
| A. | 该电池的正极板上覆盖有PbO2,负极板上覆盖有Pb | |
| B. | 该电池放电时的正极反应为PbO2(s)+4H+(aq)+SO2-4(aq)+2e-═PbSO4(s)+2H2O(l) | |
| C. | 该电池充电时,两个电极上都有PbSO4生成 | |
| D. | 用该电池电解饱和食盐水制氯气,若制得0.050molCl2,这时电池内消耗H2SO40.10mol |
15.某无色混合气体甲,可能含NO、NO2、NH3、CO2、N2中的几种,将100mL气体甲依次经过如图所示的实验处理,结果得到酸性溶液且最终无剩余气体.则气体甲的组成为( )
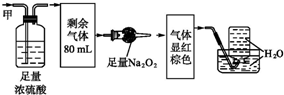

| A. | NH320ml、NO240ml、N240ml | B. | NH3 20ml、NO32ml、CO248ml | ||
| C. | NH320ml、NO20ml、CO260ml | D. | NH320ml、CO228ml、NO52ml |
12.在恒容密闭容器中进行氢气与碘(气态)合成HI的反应,下列说法能表明反应达到平衡的是( )
| A. | 气体的平均分子量不再变化 | B. | 反应的平衡常数不变 | ||
| C. | ?(H2)=2 ?(HI) | D. | 气体的颜色不再变化 |
19.下列各组物质中,所含分子数相同的是( )
| A. | 5.6LN2(标准状况)和11gCO2 | B. | 10gH2和10gO2 | ||
| C. | 9gH2O 和0.5molBr2 | D. | 22.4mlH2 (标准状况)和0.1molN2 |
16.解释下列事实的反应方程式正确的是( )
| A. | 纯碱溶液能清洗油污:CO32-+2H2O═H2CO3+2OH- | |
| B. | 铜与浓硫酸共热产生气体:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2↑ | |
| C. | 铁钉在潮湿的空气中很快被腐蚀:Fe-3e-═Fe3+ | |
| D. | 氨气遇到氯化氢时产生白烟:NH3+HCl═NH4Cl |
17.实验中需要1mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取的Na2CO3•10H2O的质量分别为( )
| A. | 1000mL,106g | B. | 1000mL,286g | C. | 950mL,100.7g | D. | 950mL,271.7g |
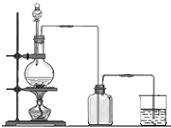 实验室用MnO2和浓盐酸反应制取Cl2,气体发生和收集装置如图.请回答:
实验室用MnO2和浓盐酸反应制取Cl2,气体发生和收集装置如图.请回答: