题目内容
17.设NA为阿伏加德罗常数的值,下列叙述错误的是( )| A. | 含14g硅原子的二氧化硅晶体中含有的硅氧键数目为2NA | |
| B. | 3.9g Na2O2晶体中含有0.2NA个离子 | |
| C. | 常温常压下,5g D2O含有的质子数、电子数、中子数均为2.5NA | |
| D. | 3mol H2和1mol N2在一定条件下反应所得混合气体分子数小于2NA |
分析 A、求出硅原子的物质的量,然后根据1mol二氧化硅中含1mol硅原子来求出二氧化硅的物质的量,然后根据1mol二氧化硅中含4mol硅氧键来分析;
B、求出过氧化钠的物质的量,然后根据过氧化钠由2个钠离子和1个阴离子构成来分析;
C、求出重水的物质的量,然后根据重水中含10个电子、10个质子和10个中子来分析;
D、合成氨的反应为可逆反应.
解答 解:A、14g硅原子的物质的量为0.5mol,而1mol二氧化硅中含1mol硅原子,故含0.5mol硅原子的二氧化硅的物质的量为0.5mol,而1mol二氧化硅中含4mol硅氧键,故0.5mol二氧化硅中含2NA条硅氧键,故A正确;
B、3.9g过氧化钠的物质的量为0.05mol,而过氧化钠由2个钠离子和1个阴离子构成,故0.05mol过氧化钠中含0.3NA个离子,故B错误;
C、5g重水的物质的量为0.25mol,而重水中含10个电子、10个质子和10个中子,故0.25mol重水中含有的质子数、中子数和电子数均为2.5NA个,故C正确;
D、合成氨的反应为可逆反应,故不能进行彻底,则所得混合物分子个数大于2NA个,故D错误.
故选BD.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.用VSEPR模型预测下列分子或离子的立体结构,其中正确的是( )
| A. | CH4与CH2Cl2均为正四面体 | B. | BeCl2与SO2为直线形 | ||
| C. | BF3与PCl3为三角锥形 | D. | NO3-与CO32-为平面三角形 |
2.设NA为阿伏加德罗常数,则下列说法正确的是( )
| A. | 标准状况下1.12L Cl2中含有的质子总数为0.85NA | |
| B. | 0.12 mol•L-1 AlCl3溶液含有0.36NA个Cl- | |
| C. | 常温常压下,9g H2O中所含原子总数为1.5NA | |
| D. | O2与O3的混合物32g,含有分子总数为NA |
9.有关同系物和同分异构体的叙述正确的是( )
| A. | 同系物的最简式相同,同分异构体的分子式相同 | |
| B. | 通式相同的是同系物,相对分子质量相同的是同分异构体 | |
| C. | 同系物的通式相同,同分异构体的相对分子质量相同 | |
| D. | 官能团相同的是同系物,含碳量相同的是同分异构体 |
6.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2 mol•L-1 的Na2SO4溶液中含有4 NA个Na+ | |
| B. | 将含有0.1 mol FeCl3的饱和溶液逐滴滴入足量沸水中,得到Fe(OH)3胶体数目为0.1 NA | |
| C. | 在标准状况下,11.2 L氖气中含有NA个氖原子1100℃ | |
| D. | 7.8 g Na2O2中阴离子数目为0.1NA |
7.下列有关化学用语表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 醛基的电子式: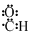 | ||
| C. | 乙酸的最简式:CH2O | D. | 乙醇分子比例模型: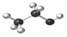 |



