题目内容
2.设NA为阿伏加德罗常数,则下列说法正确的是( )| A. | 标准状况下1.12L Cl2中含有的质子总数为0.85NA | |
| B. | 0.12 mol•L-1 AlCl3溶液含有0.36NA个Cl- | |
| C. | 常温常压下,9g H2O中所含原子总数为1.5NA | |
| D. | O2与O3的混合物32g,含有分子总数为NA |
分析 A、求出氯气的物质的量,然后根据氯气中含34个质子来分析;
B、溶液体积不明确;
C、求出水的物质的量,然后根据水为三原子分子来分析;
D、氧气和臭氧的摩尔质量不同.
解答 解:A、标况下1.12L氯气的物质的量为0.05mol,而氯气中含34个质子,故0.05mol氯气中含0.17NA个质子,故A错误;
B、溶液体积不明确,故溶液中的氯离子的个数无法计算,故B错误;
C、9g水的物质的量为0.5mol,而水为三原子分子,故0.5mol水中含1.5NA个,故C正确;
D、氧气和臭氧的摩尔质量不同,故32g氧气和臭氧的混合物的物质的量无法计算,故分子个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
相关题目
12.下列说法不正确的是( )
| A. | 任何分子或化合物都是通过原子间形成化学键相结合的 | |
| B. | 物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量 | |
| C. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| D. | 分子的稳定性与化学键强弱有关 |
10.室温下,关于1.0mL 0.l mol/L氨水,下列判断正确的是( )
| A. | 溶液的pH等于13 | |
| B. | 加入少量NH4Cl固体,c(OH-)不变 | |
| C. | c(OH-)=c(NH4+)+c(H+) | |
| D. | 与1.0 mL 0.l mol/L盐酸混合后,溶液呈中性 |
17.设NA为阿伏加德罗常数的值,下列叙述错误的是( )
| A. | 含14g硅原子的二氧化硅晶体中含有的硅氧键数目为2NA | |
| B. | 3.9g Na2O2晶体中含有0.2NA个离子 | |
| C. | 常温常压下,5g D2O含有的质子数、电子数、中子数均为2.5NA | |
| D. | 3mol H2和1mol N2在一定条件下反应所得混合气体分子数小于2NA |
7.密闭容器中分别盛有以下各选项的物质,其中一定为纯净物的是( )
| A. | 二氟甲烷 | B. | 二溴乙烷 | C. | 二甲基苯 | D. | 2-丁烯 |
14.实验室用如图所示装置制备氯气并进行性质实验(必要时可加热,省略夹持装置).
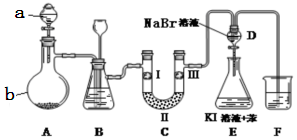
(1)仪器a的名称是:分液漏斗;装置B中长颈漏斗的作用是:平衡装置中压强,防止玻璃仪器破裂.蒸馏烧瓶b中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)洗气装置B试剂是饱和食盐水,其作用是除去氯气中的氯化氢气体,分液漏斗D中发生反应的化学方程式为Cl2+2NaBr=Br2+2NaCl.
(3)装置C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,设计C装置的目的是验证氯气还是次氯酸具有漂白性.
(4)F处为尾气吸收装置,写出实验室利用烧碱溶液吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(5)实验结束后将产生的氯气通入含紫色石蕊溶液的试管里,请填写表中的空白:

(1)仪器a的名称是:分液漏斗;装置B中长颈漏斗的作用是:平衡装置中压强,防止玻璃仪器破裂.蒸馏烧瓶b中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)洗气装置B试剂是饱和食盐水,其作用是除去氯气中的氯化氢气体,分液漏斗D中发生反应的化学方程式为Cl2+2NaBr=Br2+2NaCl.
(3)装置C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,设计C装置的目的是验证氯气还是次氯酸具有漂白性.
(4)F处为尾气吸收装置,写出实验室利用烧碱溶液吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(5)实验结束后将产生的氯气通入含紫色石蕊溶液的试管里,请填写表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成HClO具有漂白性 |
| 然后溶液从无色逐渐变为浅黄绿色 | 过量氯气溶解于水中 |
11.向含有物质的量均为0.01mol的NaOH和 Na2CO3的混合溶液中逐滴滴加a L 0.01mol•L-1的稀盐酸.下列说法不正确的是( )
| A. | 当a=1时,发生的离子反应为:OH-+H+═H2O | |
| B. | 当a=2时,发生的离子反应为:OH-+CO32-+2H+═HCO3-+H2O | |
| C. | 当1<a<2,反应后的溶液中CO32-和HCO3-的物质的量之比为:(a×10-2-0.01):(0.02-a×10-2) | |
| D. | 当a≥3时,发生的离子反应:3H++OHˉ+CO32-═2H2O+CO2↑ |
12.下列有机物命名正确的是( )
| A. | 3,3-二甲基丁烷 | B. | 3,3,4-三甲基戊烷 | ||
| C. | 2,3-二甲基-4-戊烯 | D. | 3-甲基-1-戊烯 |
 、
、 、
、 ;属于芳香醚类的是C6H5OCH3.
;属于芳香醚类的是C6H5OCH3.