题目内容
16.下列各组叙述中,有错误的是( )| A. | 钙、铁、锌、硒都是人体必需的微量元素 | |
| B. | 发现煤气泄漏应立即关闭阀门,开窗通风 | |
| C. | 用肥皂水可鉴别硬水和软水 | |
| D. | 氢能源的大量应用需解决制取成本高、贮存困难等问题 |
分析 A、钙属于常量元素;
B、发现煤气泄漏应立即关闭阀门,开窗通风,防止爆炸;
C、硬水与肥皂水混合有较多浮渣,无泡沫,软水与肥皂水混合有较多泡沫,无浮渣;
D、氢气制备成本高,贮存困难.
解答 解:A、钙属于常量元素,不是微量元素,故A错误;
B、发现煤气泄漏应立即关闭阀门,为了防止爆炸,应开窗通风,故B正确;
C、用肥皂水可鉴别硬水和软水,原因是硬水与肥皂水混合有较多浮渣,无泡沫,软水与肥皂水混合有较多泡沫,无浮渣,故C正确;
D、氢气制备成本高,贮存困难,所以氢能源的大量应用需解决制取成本高、贮存困难等问题,故D正确;
故选A.
点评 本题主要考查了化学与生活,化学服务于生活、生产,难度不大,注意对应知识的掌握.

练习册系列答案
相关题目
6.将100mL质量分数为14%的Ba(OH)2溶液的物质的量浓度稀释至原来的一半,下列稀释方法正确的是( )
| A. | 往原溶液中加100mL水 | B. | 再加100mL原溶液 | ||
| C. | 将原溶液稀释为200mL | D. | 加入等浓度等体积的硫酸 |
7.自来水处理剂经历三代变化,第一代氯气,第二代二氧化氯,第三代高铁酸钾(K2FeO4).高铁酸钾是一种新型、高效、多功能绿色水处理剂,无二次水体污染.工业制备高铁酸钠的方法之一为2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2,下列说法正确的是( )
| A. | 该反应的还原剂只有FeSO4 | |
| B. | 每生成1mol Na2FeO4只转移5mol的电子 | |
| C. | K2FeO4作为水处理剂时仅起杀菌消毒的作用 | |
| D. | 该反应在水溶液中进行并不影响高铁酸钾的生产 |
4.建立宏观和微观之间的联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
| A. | 水的三态变化--分子的间隔和排列方式发生了改变 | |
| B. | 闻到远处饭菜的香味--分子在不断的运动 | |
| C. | 水通电分解--分子在化学变化中可以再分 | |
| D. | 夏天钢轨之间的缝隙变小--原子受热时体积变大 |
11.【探究一:该白色固体的成分】
“滴水生火”魔术是用胶头滴管将水滴到包裹淡黄色固体过氧化钠的棉花上,棉花燃烧起来,淡黄色固体完全变为白色固体.滴水时发生反应:2Na2O2+2H2O﹦4NaOH+O2↑
某兴趣小组对该白色固体的成分及含量进行探究.
探究一:该白色固体的成分
猜想Ⅰ:该白色固体为氢氧化钠
猜想Ⅱ:该白色固体为碳酸钠
猜想Ⅲ:该白色固体为氢氧化钠与碳酸钠的混合物
(1)经分析,上述猜测Ⅰ不合理.
(2)为确定该白色固体的成分,小明同学设计了如下实验方案,请你一起完成下列实验报告:(实验室可供选择的试剂有:氯化钡溶液、酚酞、澄清石灰水、稀盐酸)
“滴水生火”魔术是用胶头滴管将水滴到包裹淡黄色固体过氧化钠的棉花上,棉花燃烧起来,淡黄色固体完全变为白色固体.滴水时发生反应:2Na2O2+2H2O﹦4NaOH+O2↑
某兴趣小组对该白色固体的成分及含量进行探究.
探究一:该白色固体的成分
猜想Ⅰ:该白色固体为氢氧化钠
猜想Ⅱ:该白色固体为碳酸钠
猜想Ⅲ:该白色固体为氢氧化钠与碳酸钠的混合物
(1)经分析,上述猜测Ⅰ不合理.
(2)为确定该白色固体的成分,小明同学设计了如下实验方案,请你一起完成下列实验报告:(实验室可供选择的试剂有:氯化钡溶液、酚酞、澄清石灰水、稀盐酸)
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品溶于水,加入过量的氯化钡溶液; | 白色沉淀产生 | 该反应的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl |
| ②将上述反应后的混合液过滤,取滤液加入酚酞试液. | 溶液变红色 | 证明猜想Ⅲ成立 |
1.某化学兴趣小组学习酸碱中和反应后,对稀盐酸与氢氧化钠溶液混合后的有关问题,进行了如下探究,请你一起参与他们的探究.
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
写出其中的方程式:Na2CO3+CuSO4+H2O=CO2↑+Cu(OH)2↓+Na2SO4.
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | 紫色石蕊溶液变红色 | 丙同学的猜想正确 |
| 取反应后的溶液于试管中,硫酸铜溶液 | 有蓝色沉淀生成 | 你的猜想正确 |
8.向200mL 2mol•L-1 HNO3溶液中逐渐加入铁粉至过量(假设生成的气体只有一种),在此过程中,n(Fe2+)随n(Fe)的变化如图所示.下列有关说法正确的是( )

| A. | 该过程中产生标准状况下4.48L H2 | |
| B. | 向c点处的反应液中加入稀盐酸后无明显现象 | |
| C. | 图中a=1.5 | |
| D. | 当加入铁粉n mol时(0.1<n<0.15),溶液中n(Fe3+)=(0.3-2n)mol |
12.下列含有非极性键的离子化合物是( )
| A. | CaH2 | B. | H2O2 | C. | Na2O2 | D. | KOH |
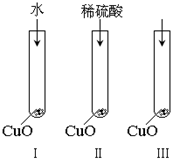 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.