题目内容
11.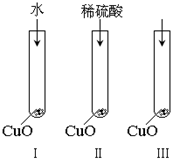 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.(1)某同学提出的假设是:H2O、H+、SO42-中的某一种粒子能够使CuO溶解;
(2)通过实验Ⅰ可以证明:水不能溶解CuO;
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的确认为:在Ⅲ中先加入Na2SO4溶液,再加入稀硫酸.
(4)探究结果为:氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O,SO42-两种粒子都不能使CuO溶解.
你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是硝酸或盐酸.
分析 根据所学知识可知稀硫酸中存在H+、SO42-、H2O三种粒子,提出假设并不困难,一般都知道应是三种粒子中的某一种使CuO溶解;关键是通过三组不同实验,根据不同的现象进行分析、对比得出是H+使CuO溶解的结论.题目中的Ⅰ实验证明了H2O不能使CuO溶解的结论,实验Ⅱ中既有H+,又有SO42-和H2O,其中水分子已经证明了不能使CuO溶解,因此实验Ⅲ就应该考虑单独含有H+或SO42-的物质和CuO反应,观察CuO是否溶解,所以实验Ⅲ中应加入的物质可以是稀盐酸或硫酸钠溶液,还能溶解CuO的另一种常见物质是硝酸或盐酸.
解答 解:(1)稀硫酸中存在H+、SO42-、H2O三种粒子,所以提出的假设为:H2O、H+、SO42-中的某一种粒子能够使CuO溶解,
故答案为:H2O、H+、SO42-中的某一种粒子能够使CuO溶解;
(2)因为现象是氧化铜不溶解,所以结论是水分子不能使氧化铜溶解,
故答案为:水不能溶解CuO;
(3)因为Ⅰ实验证明了H2O不能使CuO溶解的结论,实验Ⅱ中既有H+,又有SO42-和H2O,其中水分子已经证明了不能使CuO溶解,而且知道实验Ⅱ中的现象是氧化铜溶解,但三个实验必须得出实验结果,所以实验Ⅲ中应加入的物质应该是含硫酸根的溶液,进而排除硫酸根是否能溶解氧化铜的结论,再加入稀硫酸提供氢离子,
故答案为:Na2SO4溶液;稀硫酸;
(4)通过实验可以得知,水分子和硫酸根离子都不能使氧化铜溶解,使氧化铜溶解的是氢离子,只有含有大量氢离子的溶液才可以和氧化铜反应使之溶解,所以结论是:稀H2SO4中的H+熔解CuO,H2O和SO42-不能溶解CuO;还能溶解CuO的另一种常见物质是硝酸或盐酸,
故答案为:氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O,SO42-两种粒子都不能使CuO溶解; 硝酸或盐酸.
点评 本题主要考查了酸溶液和氧化铜反应原理,题目难度中等,明确实验目的及发生反应原理为解答关键,试题培养了学生分析问题、解决问题的能力.

| A. | 钙、铁、锌、硒都是人体必需的微量元素 | |
| B. | 发现煤气泄漏应立即关闭阀门,开窗通风 | |
| C. | 用肥皂水可鉴别硬水和软水 | |
| D. | 氢能源的大量应用需解决制取成本高、贮存困难等问题 |
 )中所含有的共价键数目为( )
)中所含有的共价键数目为( )| A. | NA | B. | 0.7NA | C. | 1.9NA | D. | 7NA |
| A. | 升高温度,AgCl的溶解度减小 | |
| B. | 在任何含AgCl固体的水溶液中,c(Ag+)=c(Cl-)且二者乘积是一个常数 | |
| C. | AgCl沉淀生成和溶解不断进行,但速率相等 | |
| D. | 向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解的质量不变 |
| A. | CH3CH2CH3 | B. | CH3CH(CH3)2 | C. | C (CH3)4 | D. | CH3CH2 CH2CH3 |
| A. | 按照有机物系统命名法,化合物的名称为:3,3-二乙基戊烷 | |
| B. | 分子式为C4H8O2的所有酯类的同分异构体共有6种 | |
| C. | 等物质的量的乙烯与碳酸二甲酯(CH3OCOOCH3)完全燃烧消耗氧气的量相同 | |
| D. | 丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,但它们与足量的氢气充分反应后的产物是同系物 |
 实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:
实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题: