题目内容
肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物.
①NH3分子的空间构型是 ;N2H4分子中氮原子轨道的杂化类型是 .
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g) 若该反应中有4mol N-H键断裂,则形成的π键有 mol.
③肼能与硫酸反应生成N2H6SO4.N2H6SO4化学键类型与硫酸铵相同,则N2H6SO4晶体内不存在 (填标号)
a.离子键 b.共价键 c.配位键 d.范德华力.
①NH3分子的空间构型是
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g) 若该反应中有4mol N-H键断裂,则形成的π键有
③肼能与硫酸反应生成N2H6SO4.N2H6SO4化学键类型与硫酸铵相同,则N2H6SO4晶体内不存在
a.离子键 b.共价键 c.配位键 d.范德华力.
考点:判断简单分子或离子的构型,物质结构中的化学键数目计算,化学键,原子轨道杂化方式及杂化类型判断
专题:
分析:①根据价层电子对互斥理论确定分子空间构型和原子的杂化方式;
②根据1分子N2中含有2个π键,根据N-H与生成的氮气的关系式计算;
③根据硫酸铵晶体中存在的化学键判断.
②根据1分子N2中含有2个π键,根据N-H与生成的氮气的关系式计算;
③根据硫酸铵晶体中存在的化学键判断.
解答:
解:①NH3分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型;N2H4分子中氮原子的加成电子对=3+1=4,含有一个孤电子对,N原子轨道的杂化类型是sp3,故答案为:三角锥型;sp3;
②1mol氮气分子中含有2molπ键,若该反应中有4mol-H键断裂,即有1mol肼参加反应,生成1.5mol氮气,所以形成的π键有1.5mol×2=3mol,故答案为:3;
③硫酸铵是离子化合物,硫酸铵中存在离子键和共价键,N2H6SO4晶体类型与硫酸铵相同,所以N2H6SO4的晶体内存在离子键、共价键和配位键,不含范德华力,
故答案为:d.
②1mol氮气分子中含有2molπ键,若该反应中有4mol-H键断裂,即有1mol肼参加反应,生成1.5mol氮气,所以形成的π键有1.5mol×2=3mol,故答案为:3;
③硫酸铵是离子化合物,硫酸铵中存在离子键和共价键,N2H6SO4晶体类型与硫酸铵相同,所以N2H6SO4的晶体内存在离子键、共价键和配位键,不含范德华力,
故答案为:d.
点评:本题考查了价层电子对互斥理论、π键数目的计算、晶体中存在的化学键等知识,知识点较多,难度中等,要注意基础知识的积累.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
下列实验操作,正确的是( )
| A、中和滴定时,用标准液润洗滴定管,用待测液润洗锥形瓶,并滴入l mL指示剂 |
| B、配制物质的量浓度溶液时,将称量好的溶质溶于盛有适量水的烧杯中,溶解后立即倾入容量瓶中,继续进行洗涤和定容 |
| C、制取Fe(OH)2时,吸取NaOH溶液的胶头滴管的末端应插入FeSO4溶液中,再缓缓将NaOH溶液挤出 |
| D、溴乙烷和烧碱溶液共热后,将硝酸银溶液滴入水解液中,即可见到淡黄色沉淀 |
如图图示与对应叙述相符合的是( )
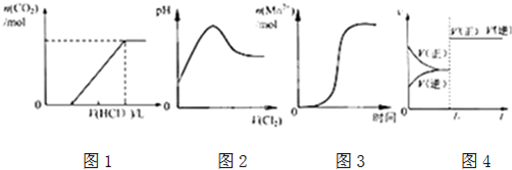

| A、图1表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol?L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 |
| B、图2表示Cl2通入H2S溶液中pH的变化 |
| C、图3表示10 mL 0.01 mol?L-1KMnO4 酸性溶液与过量的0.1 mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用) |
| D、图4表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |
用四氯化碳萃取碘水中的碘,下列说法中不正确的是( )
| A、实验中使用的主要仪器是分液漏斗 |
| B、碘在四氯化碳中的溶解度比在水中的溶解度大 |
| C、不可把萃取剂四氯化碳换成酒精 |
| D、分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从分液漏斗上口倒出 |
 (1)某矿石由几种常见氧化物组成,组成这些氧化物的元素在地壳中的含量都很丰富.向该矿石混合粉末中加入过量的氢氧化钠溶液,过滤得可用作红色涂料的红棕色固体和无色溶液,然后向所得溶液中滴入盐酸,所得沉淀的质量与所加盐酸的体积的关系如图所示:
(1)某矿石由几种常见氧化物组成,组成这些氧化物的元素在地壳中的含量都很丰富.向该矿石混合粉末中加入过量的氢氧化钠溶液,过滤得可用作红色涂料的红棕色固体和无色溶液,然后向所得溶液中滴入盐酸,所得沉淀的质量与所加盐酸的体积的关系如图所示: 变色龙的外表随环境变化时一种生物的适应性,保护色在军事上用于进行“地表伪装”一直备受战争专家的青睐,BAFS是最近开发的芘系新型红外伪装还原染料,该染料为橄榄色或黑色,其化学结构如图,当n=3时,其一氯代物(不考虑醇羟基被取代)可能有( )
变色龙的外表随环境变化时一种生物的适应性,保护色在军事上用于进行“地表伪装”一直备受战争专家的青睐,BAFS是最近开发的芘系新型红外伪装还原染料,该染料为橄榄色或黑色,其化学结构如图,当n=3时,其一氯代物(不考虑醇羟基被取代)可能有( )