题目内容
11.课题式课堂教学是研究性学习的一种方式,其基本教学模式为:提出课题→确定研究方案→解决问题→总结和评价下面是关于“一氧化碳的化学性质”的课题式课堂教学中解决问题阶段甲同学设计的证明CO具有还原性的实验装置:
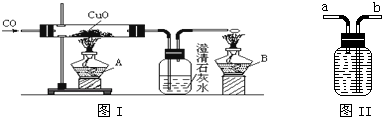
(1)点燃酒精灯A、B的先后顺序为:先B;后A.
(2)硬质玻璃管中发生的反应的化学方程式为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 ;
(3)洗气瓶中的实验现象为澄清石灰水变浑浊;
(4)酒精灯B的作用为点燃未反应的CO,防止污染环境;
(5)乙同学提出甲装置太复杂,可将酒精灯合二为一,去掉B,而将尾气导气管出口旋转到A的火焰上即可,乙同学的设计是否合理?简述理由(从A、B使用的一致性角度考虑).不合理;因为CO点燃在前,CuO加热在后,不能同时进行,否则可能引起爆炸.
(6)丙同学认为甲装置有待优化,如尾气可先储存在瓶内,然后再处理,图II是他设计的贮气瓶,尾气应从a(选a、b)口通入.
(7)丁同学质疑:CO能否使澄清石灰水变浑浊?因此,其设计在CO通入CuO之前,应先通入澄清石灰水,以比较排除CO与澄清石灰水反应.试对此作出评价,你认为丁的设计不必要(填“必要”或“不必要”).
分析 (1)实验开始需要先用CO把装置中空气赶净,一氧化碳有毒污染空气需要尾气处理;
(2)硬质玻璃管中发生的反应为一氧化碳还原氧化铜生成铜和二氧化碳,结合反应物和生成物书写化学方程式;
(3)一氧化碳还原氧化铜后生成能使澄清石灰水变浑浊的气体;
(4)一氧化碳有毒,不能直接排放到空气中.
(5)从操作顺序分析判断,一氧化碳遇到空气点燃易发生爆炸;
(6)储气装置需要导气管短进长出;
(7)加热CuO前必须先通CO,此时即可观察CO是否能使澄清石灰水变浑浊.
解答 解:(1)实验开始需要先用CO把装置中空气赶净,一氧化碳有毒污染空气需要尾气处理,点燃酒精灯A、B的先后顺序为:先点燃酒精灯B,后点燃酒精灯A,
故答案为:B;A;
(2)硬质玻璃管中发生的反应为一氧化碳还原氧化铜生成铜和二氧化碳,化学方程式为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 ,
故答案为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
(3)一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,洗气瓶中的实验现象为:澄清石灰水变浑浊,
故答案为:澄清石灰水变浑浊;
(4)CO有毒,不能直接排放,用酒精灯点燃未反应的CO,可防止污染环境,酒精灯B的作用为点燃未反应的CO,防止污染环境,
故答案为:点燃未反应的CO,防止污染环境;
(5)将酒精灯合二为一,将尾气导管出口旋转到A的火焰上的做法不合理,因为CO点燃在前,CuO加热在后,不能同时进行,否则可能引起爆炸,
故答案为:不合理;因为CO点燃在前,CuO加热在后,不能同时进行,否则可能引起爆炸;
(6)用此装置贮存气体,就要把水排出,导气管需要短进长出,排水应从a进入气体,故答案为:a;
(7)在CO通人CuO前应先通入澄清石灰水的设计不必要,因为加热CuO前必须先通CO,此时即可观察CO是否能使澄清石灰水变浑浊.
故答案为:不必要.
点评 本题考查了实验基本操作、实验顺序的分析判断,解答本题要熟悉课本上相应的实验,能根据气体的性质和操作的目的进行相应的判断,从而得出正确答案,题目难度中等.

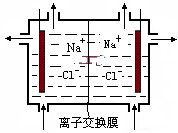
| A. | 离子交换膜既能让Na+通过,又能让OH-通过 | |
| B. | 阳极产生氯气和氢氧化钠 | |
| C. | 阴极区要定时添加饱和食盐水 | |
| D. | 阴极区流出的是氢氧化钠和氯化钠的混合溶液 |
| A. | C60是一种新型的化合物 | B. | C60的熔点高于石墨 | ||
| C. | C60和石墨都是碳的同素异形体 | D. | C60的摩尔质量为720 |
| A. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| B. | HF、HCl、HBr、HI的热稳定性依次增强 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
| A. | Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | 向NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 向AlCl3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 用铜除去CuCl2 溶液中少量的FeCl3:Fe2++Cu═Fe3++Cu2+ |
 单质A、B、C与化合物甲、乙之间有如图所示的转化关系(部分产物已省略).
单质A、B、C与化合物甲、乙之间有如图所示的转化关系(部分产物已省略).