题目内容
16.下列说法正确的是( )| A. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| B. | HF、HCl、HBr、HI的热稳定性依次增强 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
分析 A.离子键中存在静电引力和静电斥力;
B.非金属性越强,氢化物的稳定性越强;
C.必须指出最高价氧化物对应的含氧酸,否则该说法不一定成立;
D.结构决定性质,元素原子核外电子排布周期性变化引起性质的变化.
解答 解:A.形成离子键的阴阳离子间既存在静电吸引力也存在静电斥力,故A错误;
B.非金属性F>Cl>Br>I,则氢化物的HF、HCl、HBr、HI的热稳定性依次减弱,故B错误;
C.第三周期非金属元素的最高价氧化物对应的水合物的酸性从左到右依次增强,必须指出最高价含氧酸,故C错误;
D.元素的结构决定了元素的性质,则元素周期律是元素原子核外电子排布周期性变化的结果,故D正确;
故选D.
点评 本题考查较为综合,涉及元素周期律的内容及应用、离子键等知识,明确原子结构与元素周期律的关系为解答关键,注意掌握化学键的类型及存在作用力,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
6.下述实验设计能够达到目的是( )
| A. | SO2中混有少量SO3,通过足量浓硫酸,收集气体 | |
| B. | HNO3溶液中混有少量H2SO4,加入适量BaCl2溶液,再过滤 | |
| C. | 提取溴水中的溴,可用加入乙醇萃取的方法 | |
| D. | 检验溶液中是否含有Fe2+,向溶液中滴入氯水后,再滴加KSCN溶液 |
4.类推的思想方式在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证.以下类推的结论中正确的是( )
| A. | SO2能使酸性KMnO4溶液褪色,故CO2也能使酸性KMnO4溶液褪色 | |
| B. | 盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气 | |
| C. | SO2能使品红溶液褪色,故CO2也能使品红溶液褪色 | |
| D. | 常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化 |
1.下列变化属于化学变化的是( )
①导电性;②瓦斯爆炸;③缓慢氧化;④丁达尔效应;⑤萃取;⑥焰色反应.
①导电性;②瓦斯爆炸;③缓慢氧化;④丁达尔效应;⑤萃取;⑥焰色反应.
| A. | ①②④ | B. | ②③ | C. | ②③⑥ | D. | ②③⑤ |
5.下列指定反应的离子方程式正确的是( )
| A. | 向Na2O2中加入足量水:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| B. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH4+ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
6.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向Na2SiO3溶液中滴加几滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| B | 取久置的Na2O2粉末,向其中滴加过量的盐酸后产生气体 | Na2O2没有变质 |
| C | 溴乙烷与NaOH溶液共热后,加入AgNO3溶液,未出现淡黄色沉淀 | 溴乙烷没有水解 |
| D | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32-强 |
| A. | A | B. | B | C. | C | D. | D |
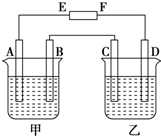 在图中,E和F分别为电源两极;甲烧杯中盛有100mL 0.2mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.15mol•L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则
在图中,E和F分别为电源两极;甲烧杯中盛有100mL 0.2mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.15mol•L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则