题目内容
10.等质量的C2H4与C3H6所含的分子数之比为3:2,原子数之比为1:1,H原子数之比为1:1.分析 质量相同时,根据N=$\frac{m}{M}{N}_{A}$计算其分子数之比,二者的最简式相等,二者的质量相等、最简式相等,所以其最简式的物质的量相等,原子个数相等.
解答 解:根据N=$\frac{m}{M}{N}_{A}$知,质量相同时,二者的分子数之比等于摩尔质量的反比,即分子数之比为=42g/mol:28g/mol=3:2,二者的质量相等、最简式相等,所以其最简式的物质的量相等,原子个数相等,则原子个数之比为1:1,分子数之比等于物质的量之比,为3:2,H原子数之比为1:1,
故答案为:3:2;1:1,1:1.
点评 本题考查物质的量的有关计算,明确物质的量公式中各个物理量的关系是解本题关键,熟练掌握物质的量的有关公式,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) 表示,则正确的关系是( )
| A. | 4 v(NH3)=5 v(O2) | B. | 5 v(O2)=6 v(H2O) | C. | 4 v(O2)=5 v(NO) | D. | 2 v(NH3)=3 v(H2O) |
1.把6.2gNa2O溶于93.8g水中;把4.6g金属钠溶于95.6g水中;把7.8gNa2O2溶于93.8g水中,把8gNaOH溶于92g水中.得到的溶液的质量分数( )
| A. | 都是8% | B. | 分别为8%、8%、7%、10% | ||
| C. | 都是9% | D. | 分别为6%、7%、8%、10% |
5.下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑥CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
⑦HF、HCl、HBr、HI的热稳定性依次减弱.
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑥CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
⑦HF、HCl、HBr、HI的热稳定性依次减弱.
| A. | ①②③④⑤ | B. | ①②③⑤ | C. | ①②③④ | D. | ①②③ |
15.用NA表示阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1mol乙基(-CH2CH3)中含有共价键的总数为7NA | |
| B. | 1L 0.1mol/L盐酸溶液所含HCl的分子数为NA | |
| C. | 标准状况下,11.2L NO2气体中含有的分子数为0.5NA | |
| D. | 标况下11.2L CO和CO2混合气体中,所含碳原子数为0.5NA |
 X、Y、Z、W、R.均为前四周期元素且原子序数依次增大,X的基态原子核外有7种不同运动状态的电子,Y和Z原子最外层均有2对成对电子,Z的原子序数为Y的原子序数的2倍,W3+的基态离子3d轨道为半充满状态,R的氢氧化物悬浊液可用于检验葡萄糖的存在.
X、Y、Z、W、R.均为前四周期元素且原子序数依次增大,X的基态原子核外有7种不同运动状态的电子,Y和Z原子最外层均有2对成对电子,Z的原子序数为Y的原子序数的2倍,W3+的基态离子3d轨道为半充满状态,R的氢氧化物悬浊液可用于检验葡萄糖的存在.
 是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
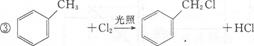
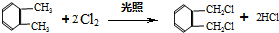 .
.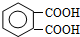 +2CH3CH2OH
+2CH3CH2OH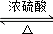
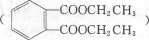 +2H2O.
+2H2O.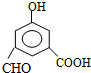 ,每种同分异构体中,化学环境不同的氢原子都是6种.
,每种同分异构体中,化学环境不同的氢原子都是6种.