题目内容
3.以苯酚为原料的合成路线如图所示,请按要求作答:
(1)写出以下列物质的结构简式:B
 F
F
(2)写出反应①④的化学反应方程式:
①
 ④
④
(3)反应⑤可以得到E,同时可能得到的副产物的结构简式为:
 .
.
分析 根据苯酚的性质可知,与氢气发生加成反应生成A为 ,
, 在浓硫酸作用下发生消去反应生成B为
在浓硫酸作用下发生消去反应生成B为 ,进而与溴发生加成反应生成C为
,进而与溴发生加成反应生成C为 ,C在NaOH乙醇溶液的作用下发生消去反应生成D为
,C在NaOH乙醇溶液的作用下发生消去反应生成D为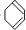 ,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由G可知应为1,4加成产物,则E为
,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由G可知应为1,4加成产物,则E为 ,F为
,F为 ,最后水解可生成G,结合有机物的结构和性质解答该题.
,最后水解可生成G,结合有机物的结构和性质解答该题.
解答 解:根据苯酚的性质可知,与氢气发生加成反应生成A为 ,
, 在浓硫酸作用下发生消去反应生成B为
在浓硫酸作用下发生消去反应生成B为 ,进而与溴发生加成反应生成C为
,进而与溴发生加成反应生成C为 ,C在NaOH乙醇溶液的作用下发生消去反应生成D为
,C在NaOH乙醇溶液的作用下发生消去反应生成D为 ,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由G可知应为1,4加成产物,则E为
,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由G可知应为1,4加成产物,则E为 ,F为
,F为 ,最后水解可生成G,
,最后水解可生成G,
(1)由以上分析可知B为 ,F为
,F为 ,故答案为:
,故答案为: ;
; ;
;
(2)反应①为苯酚与氢气发生加成反应生成 ,反应的方程式为
,反应的方程式为 ,反应④为
,反应④为 在NaOH乙醇溶液的作用下发生消去反应生成
在NaOH乙醇溶液的作用下发生消去反应生成 ,方程式为
,方程式为 ,
,
故答案为: ;
; ;
;
(3)D为 ,与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,对应的副产品为
,与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,对应的副产品为 ,
,
故答案为: .
.
点评 本题考查有机物的推断,题目难度不大,解答本题的关键是根据苯酚能发生加成反应的性质进行推断.

练习册系列答案
相关题目
11.下列离子方程式书写正确的是( )
| A. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 钠与水的反应Na+2H2O=Na++2OH-+H2↑ | |
| C. | 铜片跟稀硝酸反应:Cu+NO3-+4H+═Cu2++NO↑+2H2O | |
| D. | 铝片和氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
14.反应H2(g)+I2(g)?2HI(g)的平衡常数K1;反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
| A. | K1=2K2 | B. | K1=K2 | C. | K1=$\frac{1}{{{K}_{2}}^{2}}$ | D. | K1=$\frac{1}{2{K}_{2}}$ |
11.下列反应中,不属于氧化还原反应的是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | B. | H2+Cl2═2HCl | ||
| C. | 2Na2O2+2CO2═2Na2CO3+O2 | D. | Fe+CuSO4═FeSO4+Cu |
18.从下列实验事实所引出的相应结论正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越长 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | H+浓度相同的盐酸和硫酸分别与等质量的形状相同的锌粒反应 | 反应开始速率相同 |
| D | 在容积可变的密闭容器中发生反应H2(g)+I2(g)?2HI(g),把容积缩小一倍 | 反应速率不变 |
| A. | A | B. | B | C. | C | D. | D |
15.以下物质:(1)甲烷;(2)苯;(3)聚乙烯;(4)苯乙烯;(5)2丁炔;(6)甲苯.既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
| A. | (1)(2)(3)(5) | B. | (4)(5) | C. | (2)(4)(5) | D. | (4)(5)(6) |
12.下列各组离子,在强碱性溶液中可大量共存的是( )
| A. | I-,AlO2-,Cl-,S2- | B. | Na+,K+,NH4+,Ba2+ | ||
| C. | Br-,HS-,Cl-,CO32- | D. | SO32-,NO3-,SO42-,HCO3- |
