题目内容
11.进行有关气体的实验时一般需要进行尾气处理,请思考应采取哪些方法对下列气体进行处理.Cl2 HCl SO2 NH3 NO2.
分析 尾气处理:对有毒气体进行回收,或通过化学方法进行反应生成无毒物质,以减轻对环境的污染,结合各物质的性质分析解答.
解答 解:进行有关气体的实验时尾气,可通过气囊进行收集,或通过溶于水吸收或通过化学方法进行处理,Cl2、HCl、SO2、NH3、NO2具体方法如下:
实验室制氯气的尾气处理用NaOH(或KOH)溶液吸收,其化学反应方程式为Cl2+2NaOH═NaCl+NaClO+H2O (或Cl2+2KOH═KCl+KClO+H2O),装置如图:
HCl是极易溶于水的气体,须用倒扣的漏斗防倒吸,装置如图: ,
,
二氧化硫可与氢氧化钠溶液反应,可用氢氧化钠溶液吸收尾气,二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH═Na2SO3+H2O,装置如图: ,
,
NH3是极易溶于水的气体,须用倒扣的漏斗防倒吸,装置如图: ,
,
NO2可以用NaOH溶液吸收或碳酸钠溶液吸收,反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O,2NO2+2Na2CO3+H2O=NaNO2+NaNO3+2NaHCO3,装置如图: ,
,
答:Cl2用NaOH(或KOH)吸收;HCl用水吸收.SO2用氢氧化钠溶液吸收,NH3 用水吸收,NO2用NaOH溶液吸收或碳酸钠溶液吸收.
点评 本题考查尾气的处理,为高频考点,把握气体的性质、化学与环境的关系为解答的关键,侧重分析与应用能力的考查,注意尾气吸收要彻底,题目难度不大.

练习册系列答案
相关题目
19.下列设计的实验方案能达到实验目的是( )
| A. | 制备Fe(OH)3胶体:在加热时,向0.1 mol•L-1FeCl3溶液中滴加NaOH溶液 | |
| B. | 配制pH=3的CH3COOH溶液:取1 mL 1 mol•L-1CH3COOH溶液加水至100 mL | |
| C. | 提纯含有少量溴的溴苯:向含有少量溴的溴苯中加入过量NaOH溶液充分振荡后,静置、分液,并除去有机相的水 | |
| D. | 比较AgCl、AgI的Ksp:向1 mL浓度均为2 mol•L-1的Cl-、I-的混合溶液中,加入1 mL 2 mol•L-1AgNO3溶液 |
20.NA表示阿伏伽德罗常数,下列判断正确的是( )
| A. | 在20g D2O中含有NA个氧原子 | |
| B. | 标准状况下,2.24 L三氧化硫中所含氧原子数为0.3 NA | |
| C. | 1 molCl2参加反应转移电子数一定为2NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1 mol/L |
9.利用铜萃取剂M,通过如下反应实现铜离子的富集(如图1):
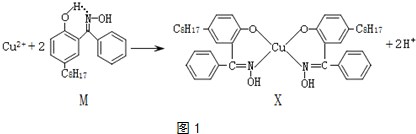
(1)X难溶于水、易溶于有机溶剂,其晶体类型为分子晶体.
(2)X中以sp2杂化、sp3杂化的原子的第一电离能由大到小顺序为N>O>C.
(3)上述反应中断裂和生成的化学键有be(填序号).
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图2)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
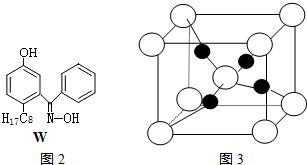
(5)硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒等功效.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表.回答下列问题:
图3是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子).
①该温度是1000℃以上.
②铜原子的配位数是4.

(1)X难溶于水、易溶于有机溶剂,其晶体类型为分子晶体.
(2)X中以sp2杂化、sp3杂化的原子的第一电离能由大到小顺序为N>O>C.
(3)上述反应中断裂和生成的化学键有be(填序号).
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图2)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.

(5)硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒等功效.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表.回答下列问题:
| 温度范围/℃ | 固体质量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
①该温度是1000℃以上.
②铜原子的配位数是4.
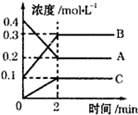 如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题:
如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题: 2B+C.
2B+C.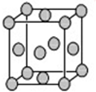 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+6ns1,回答下列问题.
某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+6ns1,回答下列问题. .填出:E原子的核外有29 种不同运动状态的电子,B和C的第一电离能大小关系N>O (用元素符号表示).
.填出:E原子的核外有29 种不同运动状态的电子,B和C的第一电离能大小关系N>O (用元素符号表示).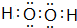 ,两种化合物可任意比互溶,解释其主要原因为H2O与H2O2之间形成氢键.
,两种化合物可任意比互溶,解释其主要原因为H2O与H2O2之间形成氢键.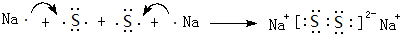 .
.