题目内容
12.下列实验操作、现象和结论均正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液 | 先有白色沉淀生成后变为蓝色沉淀 | Cu(OH)2的Ksp比Mg(OH)2的小 |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| C | 向盛Na2SiO3 溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| D | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳 | 浓硫酸具有吸水性和强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶度积常数大的物质能转化为溶度积常数小的物质;
B.K元素焰色反应必须透过蓝色钴玻璃观察;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
D.浓硫酸具有吸水性、脱水性和强氧化性.
解答 解:A.溶度积常数大的物质能转化为溶度积常数小的物质,0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液,先有白色沉淀生成后变为蓝色沉淀,说明发生沉淀的转化,则说明Cu(OH)2的Ksp比Mg(OH)2的小,故A正确;
B.K元素焰色反应必须透过蓝色钴玻璃观察,滤去黄光的干扰,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,HCl不是Cl元素最高价氧化物的水化物,所以不能比较Cl、Si非金属性强弱,故C错误;
D.浓硫酸具有吸水性、脱水性和强氧化性,该实验中浓硫酸将蔗糖中H、O元素以2:1水的形式脱去,体现浓硫酸的脱水性和强氧化性,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及溶度积大小比较、焰色反应、非金属性强弱判断、浓硫酸的性质等知识点,明确实验原理及物质性质是解本题关键,注意浓硫酸吸水性和脱水性区别,易错选项是C.

练习册系列答案
相关题目
20.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )

| A. | 该反应是吸热反应 | |
| B. | 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量 | |
| C. | 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 | |
| D. | 断裂2 mol A-B键需要吸收y kJ的能量 |
17.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
| A. | “歼-20”飞机上大量使用的碳纤维是一种新型的有机高分子材料 | |
| B. | “神舟十号”宇宙飞船返回舱外表面主要是导电导热良好的新型金属材料钛合金 | |
| C. | “天宫一号”是中国第一个空间实验室,其太阳能电池板的主要材料是硅 | |
| D. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
4.下列图示与对应的叙述相符的是( )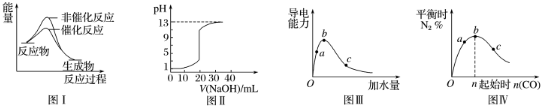

| A. | 图Ⅰ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. | 图Ⅱ表示常温下,0.100 mol•L-1 NaOH溶液滴定20.00 mL 0.100 mol•L-1 HCl溶液所得到的滴定曲线 | |
| C. | 图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c<a<b | |
| D. | 图Ⅳ表示反应4CO(g)+2NO2(g)?N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2转化率c>b>a |
 .
.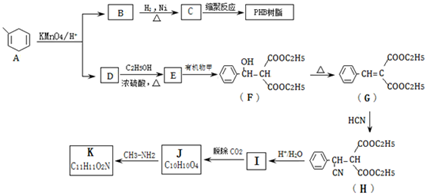
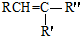 $\stackrel{KMnO_{4}/H+}{→}$RCOOH+
$\stackrel{KMnO_{4}/H+}{→}$RCOOH+
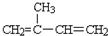 .B的结构简式是
.B的结构简式是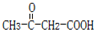 .
.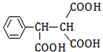 .
.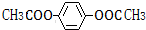 .
.
 .
.
 .
.