题目内容
18.已知:可逆反应N2(g)+3H2(g)?2NH3(g)△H<0.现有甲、乙两个容积相同且不变的真空密闭容器,向甲容器中加入1mol N2(g)和3mol H2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ.在相同条件下,向乙容器中加入2mol NH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2.下列叙述中正确的是( )| A. | Q1+Q2=92.4 | |
| B. | 达平衡时甲、乙中NH3的体积分数乙>甲 | |
| C. | 达到平衡后,再向乙中加入0.25mol N2(g)、0.75mol H2(g)和1.5mol NH3(g),平衡向生成N2的方向移动 | |
| D. | 达平衡时甲中N2的转化率为25% |
分析 由于1molN2和3molH2完全反应可以生成2molNH3,所以甲乙两个体系的平衡状态是一样的,即对应气体的浓度完全相同. 对于同一可逆反应,相同条件下,正反应的反应热与逆反应的反应热,数值相等,符号相反,N2和H2完全反应时放热Q,则NH3完全分解时吸热也是Q,
根据三段式利用x表示出平衡时甲容器内反应混合物各组分的物质的量为 N2(1-x )mol、H2(3-3x )mol、NH32xmol,放出热量Q1=xQkJ;
则乙容器反应混合物各组分的物质的量也是为 N2(1-x )mol、H2(3-3x )mol、NH32xmol,所以分解的NH3的物质的量为(2-2x)mol,吸收热量(1-x)QkJ,利用Q1=3Q2,列放出求出x的值,转化的N2为x,据此进行解答.
解答 解:由于1molN2和3molH2完全反应可以生成2molNH3,所以甲乙两个体系的平衡状态是一样的,即三种气体的浓度完全相同,对于同一可逆反应,相同条件下,正反应的反应热与逆反应的反应热,数值相等,符号相反.N2和H2完全反应时放热Q,则NH3完全分解时吸热也是Q,
假设甲容器中的参加反应的氮气的物质的量为xmol,所以:
对于甲容器:N2(g)+3H2(g)?2NH3(g)△H=-QkJ/mol
起始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以Q1=xQkJ,
乙容器反应混合物各组分的物质的量也是为N2(1-x )mol、H2(3-3x )mol、NH32xmol,所以分解的NH3的物质的量为(2-2x)mol,
对于乙容器:2NH3(g)?N2(g)+3H2(g)△H=+QkJ/mol,故吸收的热量Q2=$\frac{2-2x}{2}$×QkJ=(1-x)QkJ,
则3(1-x)Q=xQ,解得:x=0.75,
A.该反应为反应方向不同的可逆反应,则Q1+Q2=92.4,故A正确;
B.甲乙容器中达到的平衡是相同平衡,所以氨气的体积分数相同,故B错误;
C.依据分析计算得到平衡物质的量N2为0.25mol,H2为0.75mol,NH3为1.5mol,再向乙中加入0.25mol N2(g)、0.75mol H2(g)和1.5mol NH3(g),相当于增大压强,平衡正向进行,故C错误;
D.N2的转化率为:$\frac{0.75}{1}$×100%=75%,故D错误;
故选A.
点评 本题考查化学平衡的计算,题目难度中等,明确等效平衡的判断、转化率计算方法是解题关键,注意掌握化学平衡羟基影响,试题培养了学生的分析能力及化学计算能力.

| A. | 原子半径:Na>Mg>C>N | B. | 热稳定性:HI<HBr<HCl<HF | ||
| C. | 最高正化合价:Si<P<S<Cl | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3>KOH |
| A. | 标准状况下,1 L庚烷所含有的分子数为$\frac{{N}_{A}}{22.4}$ | |
| B. | 1 mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,B2H6和C2H4的混合气体22.4 L,所含的电子数约为16NA | |
| D. | 26 g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |

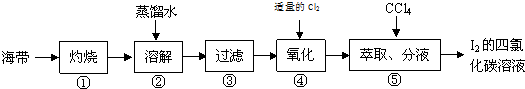
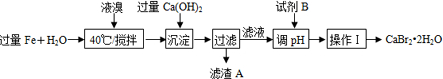
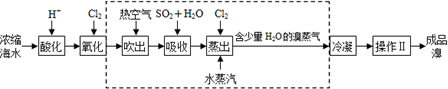
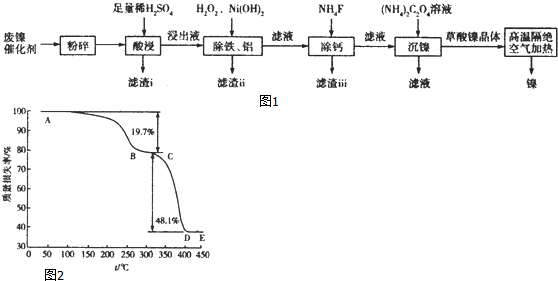
 .
.