题目内容
3.下列关于S、Si、N、Cl等非金属元素化合物的说法正确的是( )| A. | SiO2是制造太阳能电池板的主要材料 | |
| B. | NO、NO2是大气污染物,能在空气中稳定存在 | |
| C. | 漂白精的有效成分是Ca(ClO)2 | |
| D. | Fe与S化合生成Fe2S3 |
分析 A、二氧化硅是光导纤维的成份;
B、NO、NO2是大气污染物,但一氧化氮不能稳定存在;
C、利用石灰乳和氯气反应制备漂白粉,根据反应生成物及性质分析;
D、硫是弱氧化剂,Fe与S化合生成FeS.
解答 解:A、二氧化硅是光导纤维的成份,而硅是制造太阳能电池板的主要材料,故A错误;
B、NO、NO2是大气污染物,但一氧化氮不能稳定存在,与氧气生成二氧化氮,故B错误;
C、石灰乳和氯气反应制备漂白粉,该反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,生成物中CaCl2和Ca(ClO)2为漂白粉的主要成分,Ca(ClO)2为有效成分,漂白原理为:漂白粉与二氧化碳、水的反应Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,生成的次氯酸具有漂白性,故C正确;
D、硫是弱氧化剂,Fe与S化合生成FeS,而不是Fe2S3,故D错误;
故选C.
点评 题主要考查了元素化合物知识,侧重考查了硅、氯、氮的性质,题目难度不大,注意Ca(ClO)2为漂白粉的有效成分.

练习册系列答案
相关题目
14.下列各组物质在溶液中进行反应,可以用同一离子方程式表示的是( )
| A. | Na2CO3和HNO3;NaHCO3和HNO3 | B. | BaCl2和Na2CO3;Ba(OH)2和K2CO3 | ||
| C. | Ba(OH)2和NaHSO4;Ba(OH)2和H2SO4 | D. | NaOH和HF;Ba(OH)2和HNO3 |
15.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| B. | 0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| C. | 向醋酸钠溶液中加入等量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等物质的量浓度的①NH4Cl溶液 ②(NH4)2SO4溶液 ③NH4HSO4溶液④(NH4)2 CO3 溶液中NH4+浓度的大小关系是②>④>①>③ |
12.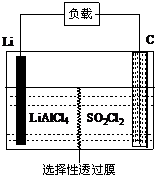 为了国防现代化,某军事科研所研发了一种新型的Li-SO2Cl2军用电池,其组成结构示意图如图所示.已知电池总反应为:2Li+SO2Cl2═2LiCl+SO2↑.下列说法中不正确的是( )
为了国防现代化,某军事科研所研发了一种新型的Li-SO2Cl2军用电池,其组成结构示意图如图所示.已知电池总反应为:2Li+SO2Cl2═2LiCl+SO2↑.下列说法中不正确的是( )
 为了国防现代化,某军事科研所研发了一种新型的Li-SO2Cl2军用电池,其组成结构示意图如图所示.已知电池总反应为:2Li+SO2Cl2═2LiCl+SO2↑.下列说法中不正确的是( )
为了国防现代化,某军事科研所研发了一种新型的Li-SO2Cl2军用电池,其组成结构示意图如图所示.已知电池总反应为:2Li+SO2Cl2═2LiCl+SO2↑.下列说法中不正确的是( )| A. | 电池的负极反应为:2Li-2e-═2Li+ | |
| B. | 工作时电流方向:锂电极→导线→负载→碳棒 | |
| C. | 正极电极反应为:SO2Cl2+2e-═2Cl-+SO2↑ | |
| D. | 电池工作时,会在碳棒表面看到气泡产生 |
 A~I为中学化学中常见的物质,B、E、F为单质,且在常温下B是一种黄绿色有毒气体,E为紫红色金属,G为黑色固体.它们的相互转化关系如图所示(部分生成物未列出).请回答下列问题:
A~I为中学化学中常见的物质,B、E、F为单质,且在常温下B是一种黄绿色有毒气体,E为紫红色金属,G为黑色固体.它们的相互转化关系如图所示(部分生成物未列出).请回答下列问题: .
.
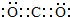 ;
; HClO+OH-;
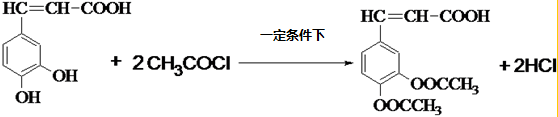
HClO+OH-;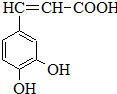 咖啡酸(如图),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
咖啡酸(如图),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.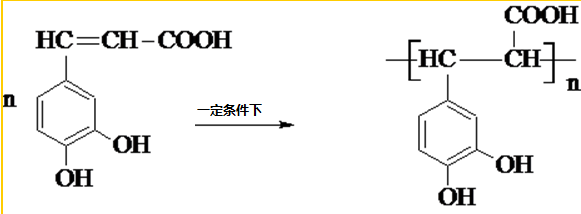 .
. .
. .
. .
.
