��Ŀ����
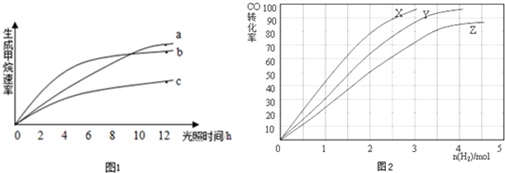
12������������Ϣ�����1����0.1mol/L�����Ը��������Һ�ⶨFeSO4��Һ��Ũ��ʱ����FeSO4��Һ����ʱ��ϳ������²ⶨ���ƫС���ƫ�������䡱��ƫС����
��2���������Ƶĵ���ʽ
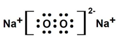
��3��ѡ������˵������ȷ�Ģݢ��
�������ﶼ�����������Һ��Ӧ
�ں챦ʯ����觡�ˮ������ʯ��װ��Ʒ����Ҫ�ɷֶ��ǹ�����
������ͬԪ����ɵ�����һ���Ǵ�����
��Ũ��ˮ�μӵ�FeCl3��Һ�п���ȡFe��OH��3����
��������ƿ��ת��Һ��ʱ�������������ԽӴ�������ƿ��ƿ��
���ò�˿պȡ����ij��Һ������ɫ��Ӧ������ʻ�ɫ������Һһ����������Һ
�߽���Mg�Ļ����Ա�Alǿ����Al2O3����NaOH��Һ��Ӧ��֪MgOҲ����NaOH��Һ��Ӧ
��SiO2���ܺ�NaOH��Һ��ӦҲ�ܺ�����ᷴӦ������������������
��3mol����Fe����������ȫת��ΪFe3O4��ʧȥ8NA������
���ú��轺�����۵���С����ʳƷһ���ܷ��װ��������Fe�۵Ļ�ԭ��
��4��Ũ������ñ��4HNO3=4NO2+O2+2H2O
��5��������Һ����������������Һ��Ӧ�����ӷ���ʽ2Al3++3SO42-+3Ba2++6OH-=2Al��OH��3��+3BaSO4����
���� ��1��FeSO4���л�ԭ�ԣ��ɱ�����������������
��2����������Ϊ���ӻ����
��3����CO�����������Һ������Ӧ��
����觡�ˮ������Ҫ�ɷ�Ϊ�������裬��ʯ����Ҫ�ɷ�ΪC��
��ͬ������������ͬԪ����ɣ�
��Ũ��ˮ�μӵ�FeCl3��Һ�п���ȡFe��OH��3������
��������ƿ��ת��Һ��ʱ�������������ԽӴ�������ƿ��ƿ�ڣ���ֹҺ��������
����ɫ��ӦΪԪ�ص����ʣ�
��MgO��NaOH��Һ����Ӧ��
��SiO2����ᷴӦ�������Σ�
��3mol����Fe����������ȫת��ΪFe3O4��Fe�Ļ��ϼ۱�Ϊ+2��+3�ۣ�ʧȥ8NA�����ӣ�
���ú��轺�����۵���С����ʳƷһ���ܷ��װ��������Fe�۵Ļ�ԭ�ԣ��ɷ�ֹʳƷ��������
��4�����ᱻ�ȶ����ֽ����ɶ���������
��5��������Һ����������������Һ��Ӧ�������������������ᱵ������
��� �⣺��1��FeSO4���л�ԭ�ԣ��ɱ��������������������ڿ����з�ֹ����������Ũ�ȼ�С���ⶨ���ƫС���ʴ�Ϊ��ƫС��
��2����������Ϊ���ӻ��������ʽΪ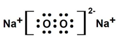 ���ʴ�Ϊ��
���ʴ�Ϊ��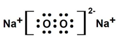 ��
��
��3����CO�����������Һ������Ӧ��Ϊ������������ʴ���
����觡�ˮ������Ҫ�ɷ�Ϊ�������裬��ʯ����Ҫ�ɷ�ΪC���ʴ���
��ͬ������������ͬԪ����ɣ�����ɻ����ʴ���
��Ũ��ˮ�μӵ�FeCl3��Һ�п���ȡFe��OH��3���������ܵõ����壬�ʴ���
��������ƿ��ת��Һ��ʱ�������������ԽӴ�������ƿ��ƿ�ڣ���ֹҺ������������ȷ��
����ɫ��ӦΪԪ�ص����ʣ���һ��Ϊ����Һ���ʴ���
��MgO��NaOH��Һ����Ӧ���ʴ���
��SiO2����ᷴӦ�������Σ���������������ʴ���
��3mol����Fe����������ȫת��ΪFe3O4��Fe�Ļ��ϼ۱�Ϊ+2��+3�ۣ�ʧȥ8NA�����ӣ�����ȷ��
���ú��轺�����۵���С����ʳƷһ���ܷ��װ��������Fe�۵Ļ�ԭ�ԣ��ɷ�ֹʳƷ������������ȷ��
�ʴ�Ϊ���ݢ�⣻
��4�����ᱻ�ȶ����ֽ����ɶ�����������Ӧ�Ļ�ѧ����ʽΪ4HNO3=4NO2+O2+2H2O���ʴ�Ϊ��4HNO3=4NO2+O2+2H2O��
��5��������Һ����������������Һ��Ӧ�������������������ᱵ��������Ӧ�����ӷ���ʽΪ2Al3++3SO42-+3Ba2++6OH-=2Al��OH�� 3��+3BaSO4����
�ʴ�Ϊ��2Al3++3SO42-+3Ba2++6OH-=2Al��OH�� 3��+3BaSO4����
���� ���⿼���Ϊ�ۺϣ���Ƕȿ���Ԫ�ػ�����֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ���������Ԫ�ػ�����֪ʶ���ۺ���������õĿ��飬�ѶȲ���ע����ػ���֪ʶ�Ļ��ۣ�

��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
��4NO2��g��+2NaCl��s��?2NaNO3��s��+2NO��g��+Cl2��g�� K1
��2NO2��g��+NaCl��s��?NaNO3��s��+ClNO��g�� K2
��2NO��g��+Cl2��g��?2ClNO��g�� K3
��K1��K2��K3֮��Ĺ�ϵΪK3=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$��
��2��T��ʱ��2NO��g��+Cl2��g��?2ClNO��g��������Ӧ���ʱ���ʽΪv��=k cn��ClNO����������ʺ�Ũ�ȵĹ�ϵ�����
| ��� | c��ClNO��/mol•L-1 | v/mol•L-1•s-1 |
| �� | 0.30 | 3.6��10-8 |
| �� | 0.60 | 1.44��10-7 |
| �� | 0.90 | 3.24��10-7 |
��3����2L�ĺ����ܱ������г���4molNO��g����2molCl2��g�����ڲ�ͬ�¶��²��c��ClNO����ʱ��Ĺ�ϵ��ͼA��
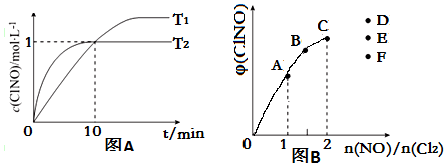
���¶�ΪT1ʱ������Ϊ�÷�Ӧ�ﵽƽ��ı�־����bdf��
a������������ֲ��� b������ѹǿ���ֲ��� c��ƽ�ⳣ��K���ֲ���
d��������ɫ���ֲ��� e��v��ClNO��=v��NO�� f��NO�� ClNO�����ʵ�����ֵ���ֲ���
�ڷ�Ӧ��ʼ��10minʱCl2��ƽ����Ӧ����v��Cl2��=0.05mol•L-1•min-1��
���¶�ΪT2ʱ��10min�Ѿ��ﵽƽ�⣬�÷�Ӧ��ƽ�ⳣ��K=2L/mol��ע����λ����
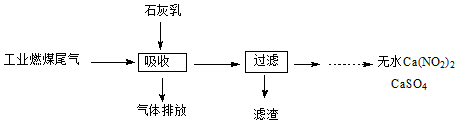
��4��һ���������ں��º��ݵ��ܱ������а�һ����������NO��g����Cl2��g����ƽ��ʱClNO�������������$\frac{n��NO��}{n��C{l}_{2}��}$�ı仯ͼ����ͼB����A��B��C��״̬�У�NO��ת������С����C�㣬��n��NO��/n��Cl2��=2.8ʱ���ﵽƽ��״̬ClNO����������տ�����D��E��F�����е�F�㣮
| A�� | �����������Ѽ�·�ˡ����������γɵ����ܽ��ж����ЧӦ | |
| B�� | ����������������֮�Ϊͭ�����ù��̷������û���Ӧ | |
| C�� | ������һ�գ���ˮ�����գ���ȡ֭���������϶������ص���ȡ���ڻ�ѧ�仯 | |
| D�� | �����ж�����̼��������������ɡ�����ЧӦ������Ҫԭ�� |
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=$\frac{c��C{O}_{2}��•c��{H}_{2}��}{c��CO��•c��{H}_{2}O��}$���÷�ӦΪ���ȷ�Ӧ�������Ȼ���ȣ������ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ���ۣ�����ţ�
��һ������ ��һ����С �ۿ������� ������С��������п���
��2�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������bc��
��a��������ѹǿ���� ��b�����������c��CO������
��c��v����H2��=v����H2O�� ��d��c��CO��=c��CO2��
��3������ͬ����CO ��g�� ��H2O ��g�� �ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO ��g��+H2O ��g��?CO2��g��+H2��g�����õ�����������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | CO2 | CO | |||
| A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| C | 1000 | 1 | 2 | c | d | t |
��ͨ�������֪��CO��ת����ʵ��A���� ʵ��B������ڡ��������ڡ���С�ڡ�����
����ʵ��C�дﵽƽ������ʱ�� tС��3������ڡ��������ڡ���С�ڡ���
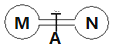 ����ʱ�������ݻ���ͬ����ƿ�зֱ�ʢ��M��N�������壨ͬ��ͬѹ����ȡ�µ��ɼ�A��ʹ����ƿ�ڵ������ֽӴ�����ͼ���������ڵ�ѹǿ�ɴ�С��˳���ǣ�������
����ʱ�������ݻ���ͬ����ƿ�зֱ�ʢ��M��N�������壨ͬ��ͬѹ����ȡ�µ��ɼ�A��ʹ����ƿ�ڵ������ֽӴ�����ͼ���������ڵ�ѹǿ�ɴ�С��˳���ǣ�������| ��� | �� | �� | �� | �� |
| ����M | H2S | NH3 | HI | NO |
| ����N | SO2 | HCl | Cl2 | O2 |
| A�� | ��=�ܣ��٣��� | B�� | �ۣ��ܣ��٣��� | C�� | �ܣ��ۣ��ڣ��� | D�� | �ܣ��ۣ��٣��� |