题目内容
2.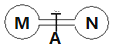 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | NH3 | HI | NO |
| 气体N | SO2 | HCl | Cl2 | O2 |
| A. | ③=④>①>② | B. | ③>④>①>② | C. | ④>③>②>① | D. | ④>③>①>② |
分析 取下弹簧夹A,使两烧瓶内的气体接触,生成的气体越少,则压强越小.
①发生2H2S+SO2=3S↓+2H2O;
②发生NH3+HCl=NH4Cl;
③Cl2+2HI=2HCl+I2,碘单质常温下是固体;
④发生2NO+O2=2NO2,设体积均为2L,结合反应分析.
解答 解:取下弹簧夹A,使两烧瓶内的气体接触,生成的气体越少,则压强越小,
①发生2H2S+SO2=3S↓+2H2O;
②发生NH3+HCl=NH4Cl;
③Cl2+2HI=2HCl+I2,碘单质常温下是固体;
④发生2NO+O2=2NO2,
设两种气体体积均为2L,
由反应可知,①中反应后只有1L气体,②不含气体,③中反应后含有3L,④中若不考虑2NO2?N2O4,则反应后得到气体体积为3L,由于部分NO2转化成N2O4,导致气体体积减小,则混合气体体积介于2-3L之间;
则容器内的压强由大到小的顺序是:③>④>①>②,
故选B.
点评 本题考查物质的量的计算,综合考查元素化合物知识,为高频考点,把握发生的反应及物质的量关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
10.对于反应2NO2(g)?N2O4(g)△H<0,在一定条件下达到平衡,欲使NO2转化率增大,应采取的措施是( )
①容器体积不变,再充入NO2
②容器体积不变,再充入N2O4
③使体积增大到原来的2倍
④升高温度.
①容器体积不变,再充入NO2
②容器体积不变,再充入N2O4
③使体积增大到原来的2倍
④升高温度.
| A. | ① | B. | ②③ | C. | ①② | D. | ③④ |
1.恒温下,在容积为2升的甲、乙两个恒容密闭容器中分别充入H2和I2发生可逆反应:H2 (g)+I2(g) 2HI(g)△H=-Q kJ/mol,实验时有关数据如表:
下列判断正确的( )
| 容器编号 | 起始物质的量mol | 4分钟后平衡时的物质量mol | 平衡时放出的热量/KJ | |
| I2 | H2 | HI | ||
| 甲 | 0.01 | 0.01 | 0.004 | Q1 |
| 乙 | 0.02 | 0.02 | a | Q2 |
| A. | 甲容器中,4分钟内氢气的反应速率为5.0×10-4rmol/(L•min) | |
| B. | 平衡时,放出的热量:Q1=4.0×10-3Q kJ | |
| C. | 平衡后,a=8.0×10-3mol,故乙中HI的质量分数比甲中高 | |
| D. | 该温度下,该反应的平衡常数K=0.25 |
5.下列现象或新技术的应用中,不涉及胶体性质的是( )
| A. | 在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 | |
| B. | 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 | |
| C. | 清晨,在茂密的树林中,常常可以看到枝叶间透过的一道道光线 | |
| D. | 肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
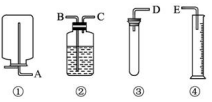 现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图
现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图