题目内容
某实验小组用下列装置进行乙醇催化氧化的实验.
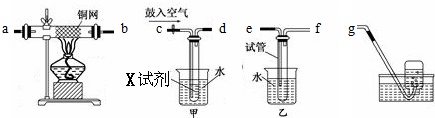
(1)X试剂是 .
(2)组装装置的顺序是c,d→ → →g.
(3)实验过程中铜网出现 的现象,请用相应的两个化学反应方程式表示出现该现象的原因 ; .
(4)甲和乙两个水浴作用不相同,甲应该应该用 (填“热”或“冷”)水浴,乙应该用 (填“热”或“冷”)水浴.
(5)反应进行一段时间后,乙装置的试管中存在的液体有乙醇、乙醛和水等,用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 .请设计一个简单可行的实验证明液体中存在的乙醛 .
(6)集气瓶中收集到的气体主要为 .

(1)X试剂是
(2)组装装置的顺序是c,d→
(3)实验过程中铜网出现
(4)甲和乙两个水浴作用不相同,甲应该应该用
(5)反应进行一段时间后,乙装置的试管中存在的液体有乙醇、乙醛和水等,用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
(6)集气瓶中收集到的气体主要为
考点:乙醇的催化氧化实验
专题:实验题
分析:(1)根据实验的原理以及各装置的用途确定X;
(2)根据实验的目的和反应发生的原理来连接;
(3)实验过程中铜网出现红色和黑色交替的现象,实验过程中铜网出现黑色,是由于铜和氧气反应生成氧化铜;铜网由黑色变成红色是由于乙醇和氧化铜反应生成铜;
(4)甲和乙两个水浴作用不相同,甲是热水浴,作用是乙醇平稳气化成乙醇蒸气,乙是冷水浴,目的是将乙醛冷却下来;
(5)能使紫色石蕊试纸变红的是酸;醛基的检验,和银氨溶液反应或和新制的氢氧化铜反应;
(6)结合空气的成分以及发生的反应确定剩余的气体成分.
(2)根据实验的目的和反应发生的原理来连接;
(3)实验过程中铜网出现红色和黑色交替的现象,实验过程中铜网出现黑色,是由于铜和氧气反应生成氧化铜;铜网由黑色变成红色是由于乙醇和氧化铜反应生成铜;
(4)甲和乙两个水浴作用不相同,甲是热水浴,作用是乙醇平稳气化成乙醇蒸气,乙是冷水浴,目的是将乙醛冷却下来;
(5)能使紫色石蕊试纸变红的是酸;醛基的检验,和银氨溶液反应或和新制的氢氧化铜反应;
(6)结合空气的成分以及发生的反应确定剩余的气体成分.
解答:
解:(1)实验室探究乙醇的催化氧化反应,需乙醇氧气为反应原料,X试剂是乙醇,将甲进行水浴加热,能使甲中乙醇平稳气化成乙醇蒸气,
故答案为:无水乙醇;
(2)实验室探究乙醇的催化氧化反应,可将甲进行水浴加热,能使甲中乙醇平稳气化成乙醇蒸气组装装置的顺序首先是c,d,则进入铜网的气体为空气和乙醇的混合气体,在加热条件下,分别发生2Cu+O2
2CuO;CH3CH2OH+CuO
CH3CHO+Cu+H2O,可观察到铜网出现红色和黑色交替的现象,组装装置的顺序其次为( a)(b );进入乙中的气体经冷却后,可在试管中得到乙醛、乙醇和水,组装装置的顺序是再次为(e )(f ),而集气瓶中收集的气体主要为氮气组装装置的顺序最后为g,
故答案为:( a)(b );(e )(f );
(3)乙醇的催化氧化反应中,金属铜作催化剂,真正和乙醇反应起到氧化作用的是氧化铜,实验过程中铜网出现黑色,是由于铜和氧气反应生成氧化铜,反应的方程式为2Cu+O2
2CuO,铜网由黑色变成红色是由于乙醇和氧化铜反应生成铜,反应的方程式为CH3CH2OH+CuO
CH3CHO+Cu+H2O,
故答案为:红色和黑色交替;2Cu+O2
2CuO;CH3CH2OH+CuO
CH3CHO+Cu+H2O;
(4)乙醇受热容易挥发,甲的作用是让乙醇以蒸汽的形式出来,乙酸在16.6℃是以晶体形式存在,所以乙的作用是将混合物冷却,
故答案为:热;冷;
(5)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,在加热条件下,乙醛和新制氢氧化铜发生氧化还原反应生成乙酸、氧化亚铜和水,体现了乙醛的还原性,实验证明液体中存在的乙醛操作为:取少量样品与新制的氢氧化铜浊液(制备时氢氧化钠过量)加热,出现砖红色说明产品中有乙醛,
故答案为:乙酸;取少量样品与新制的氢氧化铜浊液(制备时氢氧化钠过量)加热,出现砖红色说明产品中有乙醛;
(6)空气的成分主要是氮气和氧气,氧气参加反应后剩余的主要是氮气,故答案为:N2.
故答案为:无水乙醇;
(2)实验室探究乙醇的催化氧化反应,可将甲进行水浴加热,能使甲中乙醇平稳气化成乙醇蒸气组装装置的顺序首先是c,d,则进入铜网的气体为空气和乙醇的混合气体,在加热条件下,分别发生2Cu+O2
| ||
| △ |
故答案为:( a)(b );(e )(f );
(3)乙醇的催化氧化反应中,金属铜作催化剂,真正和乙醇反应起到氧化作用的是氧化铜,实验过程中铜网出现黑色,是由于铜和氧气反应生成氧化铜,反应的方程式为2Cu+O2
| ||
| △ |
故答案为:红色和黑色交替;2Cu+O2
| ||
| △ |
(4)乙醇受热容易挥发,甲的作用是让乙醇以蒸汽的形式出来,乙酸在16.6℃是以晶体形式存在,所以乙的作用是将混合物冷却,
故答案为:热;冷;
(5)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,在加热条件下,乙醛和新制氢氧化铜发生氧化还原反应生成乙酸、氧化亚铜和水,体现了乙醛的还原性,实验证明液体中存在的乙醛操作为:取少量样品与新制的氢氧化铜浊液(制备时氢氧化钠过量)加热,出现砖红色说明产品中有乙醛,
故答案为:乙酸;取少量样品与新制的氢氧化铜浊液(制备时氢氧化钠过量)加热,出现砖红色说明产品中有乙醛;
(6)空气的成分主要是氮气和氧气,氧气参加反应后剩余的主要是氮气,故答案为:N2.
点评:本题考查了乙醇的催化氧化实验,掌握乙醇的催化反应历程是解答的关键,题目难度不大.注意(2)根据实验的目的和反应发生的原理来连接为易错点.

练习册系列答案
相关题目
下列说法正确的是( )
| A、分子中含有两个氢原子的酸一定是二元酸 |
| B、向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体 |
| C、明矾可用于水的消毒、杀菌 |
| D、葡萄糖注射液不能产生丁达尔效应,不属于胶体 |
下列各组物质中,属于同系物的是( )
| A、CH3Cl CH3CH2Cl |
B、 |
| C、CH3COOH、CH3CH2OH |
| D、HCHO、CH3COOH |
下列说法正确的是( )
| A、AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 |
| B、配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 |
| C、Na2CO3溶液不可保存在带磨口塞的玻璃瓶中 |
| D、泡沫灭火器中常使用的原料是碳酸钠和硫酸铝 |
不影响H2O的电离平衡的粒子是( )
A、 | ||
B、
| ||
C、 | ||
D、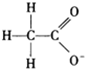 - - |
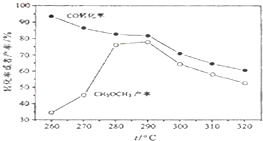 (除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图:
(除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图: