题目内容
下列说法正确的是( )
| A、分子中含有两个氢原子的酸一定是二元酸 |
| B、向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体 |
| C、明矾可用于水的消毒、杀菌 |
| D、葡萄糖注射液不能产生丁达尔效应,不属于胶体 |
考点:酸、碱、盐、氧化物的概念及其相互联系,分散系、胶体与溶液的概念及关系,胶体的重要性质,盐类水解的应用
专题:基本概念与基本理论,元素及其化合物
分析:A、能电离出的氢离子显酸性,分子中含有两个氢原子的酸不一定是二元酸;
B、向饱和FeCl3溶液中滴加过量氨水生成的是氢氧化铁沉淀;
C、明矾可以利用水解生成的氢氧化铝净水,不能用来消毒杀菌;
D、葡萄糖注射液属于溶液.
B、向饱和FeCl3溶液中滴加过量氨水生成的是氢氧化铁沉淀;
C、明矾可以利用水解生成的氢氧化铝净水,不能用来消毒杀菌;
D、葡萄糖注射液属于溶液.
解答:
解:A、能电离出的氢离子显酸性,分子中含有两个氢原子的酸不一定是二元酸,如甲酸是一元酸,故A错误;
B、向饱和FeCl3溶液中滴加过量氨水生成的是氢氧化铁沉淀,向沸水中滴加饱和氯化铁溶液加热至红褐色液体为氢氧化铁胶体,故B错误;
C、明矾可以利用水解生成的氢氧化铝净水,不能用来消毒杀菌,故C错误;
D、葡萄糖注射液属于溶液,丁达尔现象是胶体分散系的性质,故D正确;
故选D.
B、向饱和FeCl3溶液中滴加过量氨水生成的是氢氧化铁沉淀,向沸水中滴加饱和氯化铁溶液加热至红褐色液体为氢氧化铁胶体,故B错误;
C、明矾可以利用水解生成的氢氧化铝净水,不能用来消毒杀菌,故C错误;
D、葡萄糖注射液属于溶液,丁达尔现象是胶体分散系的性质,故D正确;
故选D.
点评:本题考查了物质分类的方法,胶体性质和制备,盐类水解分析应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
短周期元素X、Y、Z、R、W五种元素原子序数依次增大,其中X与Z、Y与W分别为同族元素.原子半径X<Y<W<R<Z,W原子的最外层电子数比内层电子总数少4,Z、R的核外电子数之和与Y、W核外电子数之和相等.下列说法不正确的是( )
| A、Y、Z、R的简单离子半径依次减小 |
| B、X2Y、X2Y2、X2W、WY2、WY3均为极性分子 |
| C、Y、Z、R、W四种元素中,第一电离能最小的为Z,最大的为Y |
| D、Z2Y、R2Y3、WY3的熔点由高到低的顺序 R2Y3>Z2Y>WY3 |
下列说法中不合理的是( )
| A、为使肉类保持鲜红色,加工香肠等肉类食品时应多加亚硝酸钠 |
| B、应该食用新鲜食物,少食用使用含防腐剂贮存的食物 |
| C、长期进食过量的食盐会引起高血压,使人的肾脏受损 |
| D、绝大多数食品添加剂在过量使用时对人体有害 |
下列有关范德华力叙述正确的是( )
| A、范德华力是决定由分子构成的物质的熔沸点高低的唯一因素 |
| B、范德华力是一种分子间作用力,也是一种特殊的化学键 |
| C、稀有气体原子之间不存在范德华力 |
| D、常温常压下,卤素单质从F2→I2由气态、液态到固态的原因是范德华力逐渐增大 |
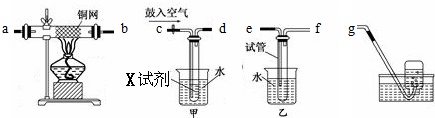
 如图所示的装置,C、D、E、F、Y都是惰性电极,X是铁电极.将电源接通一段时间后,向(乙)中滴入酚酞溶液,在F极附近显红色.以下说法不正确的是( )
如图所示的装置,C、D、E、F、Y都是惰性电极,X是铁电极.将电源接通一段时间后,向(乙)中滴入酚酞溶液,在F极附近显红色.以下说法不正确的是( )| A、欲用(丙)装置给铜镀银,G应该是Ag,电镀液是AgNO3溶液 |
| B、电源B极是负极 |
| C、装置(丁)中先有白色沉淀生成然后转化为红褐色沉淀 |
| D、(甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量比为1:1:2:2 |
 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O研读图,下列判断不正确的是( )
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O研读图,下列判断不正确的是( )| A、K 闭合时,d电极反应式PbSO4+2H2O-2e-=PbO2+4H++SO42- |
| B、当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol |
| C、K闭合时,II中SO42-向c电极迁移 |
| D、K闭合一段时间后,II可单独作为原电池,d电极为负极 |
有机化合物与我们的生活息息相关.下列说法正确的是( )
| A、甲苯的硝化、乙酸与乙醇生成乙酸乙酯的反应均可看作取代反应 |
| B、卤代烃C3H6Cl2有三种同分异构体 |
| C、石油裂解的目的是为了提高轻质液体燃料的产量和质量 |
| D、棉花和合成纤维的主要成分都是纤维素 |