题目内容
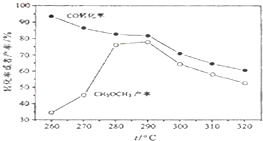 (除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图:
(除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图:(1)CO转化率随温度升高而降低的原因是
(2)在一定温度,容积不变的容器中进行该反应,则以下为达到平衡状态的标志是
a.V(CO)正:V(H2)逆=2:1
b.CO的转化率不再增大
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度
e.每断裂4molH-H键的同时形成2molH-O键
(3)二甲醚燃料电池具有启动快,效率高等优点,其能量密度高于甲醇直接燃烧利用的能量密度(5.93kW?h?kg-1),若燃料电池电解质为酸性,二甲醚燃料电池的负极反应为
考点:化学平衡状态的判断,化学电源新型电池,化学平衡的影响因素
专题:化学平衡专题,电化学专题
分析:(1)依据化学平衡移动原理分析;
(2)反应到达平衡状态时正逆反应速率相等,各物质的浓度保持不变,以及由此衍生的一些量保持不变,据此分析;
(3)燃料电池中燃料在负极上失电子发生氧化反应,书写电极反应,计算电子转移;依据能量密度=电池输出电能/燃料质量列式计算.
(2)反应到达平衡状态时正逆反应速率相等,各物质的浓度保持不变,以及由此衍生的一些量保持不变,据此分析;
(3)燃料电池中燃料在负极上失电子发生氧化反应,书写电极反应,计算电子转移;依据能量密度=电池输出电能/燃料质量列式计算.
解答:
解:(1)CO转化率随温度升高而降低,是因为反应是放热反应,升温平衡逆向进行,故答案为:反应放热,温度升高,平衡逆向移动;
(2)a.V(CO)正:V(H2)逆=2:1,之比不等于计量数之比,故不选;
b.CO的转化率不再增大,说明正逆反应速率相等,故选;
c.混合气体的平均相对分子质量不再改变,说明正逆反应速率相等,故选;
d.混合气体的密度,从反应开始一直不变,故不选;
e.每断裂4molH-H键的同时形成2molH-O键,从反应开始一直不变,故不选;
故选bc;
(3)若电解质为酸性,二甲醚直接燃料电池的负极反应为二甲醚失电子生成二氧化碳,结合原子守恒和电荷守恒写出电极反应为:CH3OCH3+3H2O-12e-=2CO2+12H+;
一个二甲醚分子经过电化学氧化失去12个电子,能量密度=电池输出电能/燃料质量,该电池的理论输出电压为1.20V,能量密度E=
=8.39KW?h?kg-1,
故答案为:CH3OCH3+3H2O-12e-=2CO2+12H+;12;
=8.39KW?h?kg-1.
(2)a.V(CO)正:V(H2)逆=2:1,之比不等于计量数之比,故不选;
b.CO的转化率不再增大,说明正逆反应速率相等,故选;
c.混合气体的平均相对分子质量不再改变,说明正逆反应速率相等,故选;
d.混合气体的密度,从反应开始一直不变,故不选;
e.每断裂4molH-H键的同时形成2molH-O键,从反应开始一直不变,故不选;
故选bc;
(3)若电解质为酸性,二甲醚直接燃料电池的负极反应为二甲醚失电子生成二氧化碳,结合原子守恒和电荷守恒写出电极反应为:CH3OCH3+3H2O-12e-=2CO2+12H+;
一个二甲醚分子经过电化学氧化失去12个电子,能量密度=电池输出电能/燃料质量,该电池的理论输出电压为1.20V,能量密度E=
1.2V×
| ||
|
故答案为:CH3OCH3+3H2O-12e-=2CO2+12H+;12;
1.2V×
| ||
|
点评:本题考查了化学平衡状态的判断,化学平衡移动原理的分析判断,原电池原理分析和电极书写,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O研读图,下列判断不正确的是( )
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O研读图,下列判断不正确的是( )| A、K 闭合时,d电极反应式PbSO4+2H2O-2e-=PbO2+4H++SO42- |
| B、当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol |
| C、K闭合时,II中SO42-向c电极迁移 |
| D、K闭合一段时间后,II可单独作为原电池,d电极为负极 |
一定条件下CuS与稀HNO3发生反应,所得还原产物为NO,氧化产物为SO
.现将0.06molCuS加入到50mL4.2mol/LHNO3中,充分反应之后,忽略溶液体积变化,下列说法正确的是( )
2- 4 |
| A、被还原的硝酸为0.08mol |
| B、反应后溶液中仍有硝酸剩余 |
| C、反应后溶液的pH=1 |
| D、CuS未全部参加反应 |
下列各项叙述中,说法不正确的是( )
| A、所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| B、镁原子由1s22s22p63s2→1s22s22p63p2时,原子吸收能量,由基态转化成激发态 |
| C、最外层电子排布为ns2np6(当只有K层时为1s2)的原子,第一电离能较大 |
| D、价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
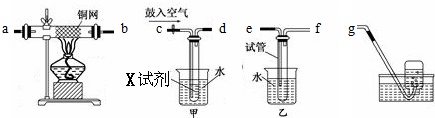
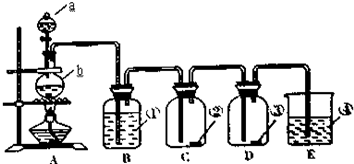
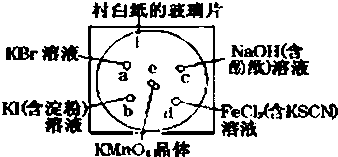
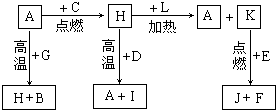 A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻.G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,K、L是无色气体,且K是非极性分子,F、H是黑色晶体.以上物质相互间的转化关系如图所示:
A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻.G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,K、L是无色气体,且K是非极性分子,F、H是黑色晶体.以上物质相互间的转化关系如图所示: