题目内容
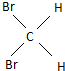
13.有机物A~M有如图转化关系,A与F分子中含碳原子数相同,且均能与NaHCO3溶液反应,F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色;D能发生银镜反应;M与NaOH溶液反应后的产物,其一氯代物只有一种.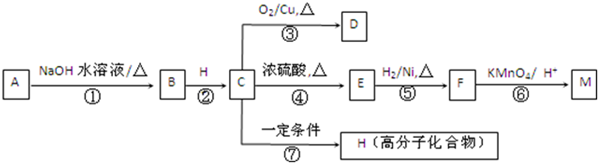
已知:
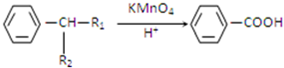 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)请回答:
(1)B、F的结构简式分别为
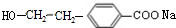 、
、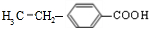 ;
;(2)反应①〜⑦中,属于消去反应的是④(填反应序号);
(3)D发生银镜反应的化学方程式为
 ;反应⑦的化学方程式为
;反应⑦的化学方程式为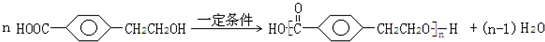 ;
;(4)A的相对分子质量在180〜260之间,从以上转化中不能确认A中的某一官能团,确 定该官能团的实验步骤和现象为取反应①后的混合液少许,向其中加入稀HNO3至酸性,滴加AgNO3溶液,若生成白色沉淀,则A中含氯原子;若生成浅黄色沉淀,则A中含溴原子;
(5)符合下列条件F的同分异构体共有2种.
a.能发生银镜反应
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6.
分析 A与F分子中所含碳原子数相同,且均能与 NaHCO3溶液反应,均含有-COOH,F的分子式为C9H10O2,不饱和度为$\frac{2×9+2-10}{2}$=5,且不能使溴的CCl4溶液褪色,不含不饱和键,应含有苯环,F发生氧化反应生成M,M与NaOH溶液反应后的产物,其一氯代物只有一种,故F中应含有乙基,且与羧基处于对位,故F为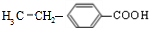 ,M为
,M为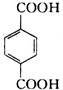 .由A→B→C的转化可知,C中含有-COOH,C发生氧化反应生成D,D能发生银镜反应,结合F的结构可知,C为
.由A→B→C的转化可知,C中含有-COOH,C发生氧化反应生成D,D能发生银镜反应,结合F的结构可知,C为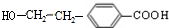 ,故D为
,故D为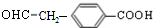 ,B为
,B为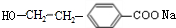 ,A的相对分子质量在180〜260之间,故A中苯环上的乙基中不可能连接羟基,应为卤素原子,A的结构为
,A的相对分子质量在180〜260之间,故A中苯环上的乙基中不可能连接羟基,应为卤素原子,A的结构为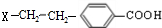 ,X相对原子质量大于180-28-76-45=31,小于260-28-76=111,X可能为Cl或Br.C发生消去反应生成E为
,X相对原子质量大于180-28-76-45=31,小于260-28-76=111,X可能为Cl或Br.C发生消去反应生成E为 ,E与氢气发生加成反应生成F.C发生缩聚反应生成高聚物H为
,E与氢气发生加成反应生成F.C发生缩聚反应生成高聚物H为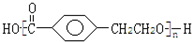 ,据此解答.
,据此解答.
解答 解:A与F分子中所含碳原子数相同,且均能与 NaHCO3溶液反应,均含有-COOH,F的分子式为C9H10O2,不饱和度为$\frac{2×9+2-10}{2}$=5,且不能使溴的CCl4溶液褪色,不含不饱和键,应含有苯环,F发生氧化反应生成M,M与NaOH溶液反应后的产物,其一氯代物只有一种,故F中应含有乙基,且与羧基处于对位,故F为 ,M为
,M为 .由A→B→C的转化可知,C中含有-COOH,C发生氧化反应生成D,D能发生银镜反应,结合F的结构可知,C为
.由A→B→C的转化可知,C中含有-COOH,C发生氧化反应生成D,D能发生银镜反应,结合F的结构可知,C为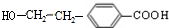 ,故D为
,故D为 ,B为
,B为 ,A的相对分子质量在180〜260之间,故A中苯环上的乙基中不可能连接羟基,应为卤素原子,A的结构为
,A的相对分子质量在180〜260之间,故A中苯环上的乙基中不可能连接羟基,应为卤素原子,A的结构为 ,X相对原子质量大于180-28-76-45=31,小于260-28-76=111,X可能为Cl或Br.C发生消去反应生成E为
,X相对原子质量大于180-28-76-45=31,小于260-28-76=111,X可能为Cl或Br.C发生消去反应生成E为 ,E与氢气发生加成反应生成F.C发生缩聚反应生成高聚物H为
,E与氢气发生加成反应生成F.C发生缩聚反应生成高聚物H为 .
.
(1)B、F的结构简式分别为 、
、 ,
,
故答案为: 、
、 ;
;
(2)反应①属于取代反应,还发生中和反应,反应②属于复分解反应,反应③⑥属于氧化反应,反应④属于消去反应,反应⑤属于加成反应,反应⑦属于缩聚反应,故答案为:④;
(3)D发生银镜反应的化学方程式为: ;
;
反应⑦的化学方程式为: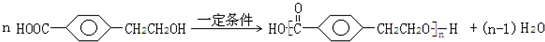 ,
,
故答案为: ;
;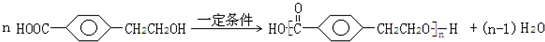 ;
;
(4)根据上面的分析可知,X可能为Cl或Br,要确定X是哪种官能团的实验步骤和现象为取反应①后的混合液少许,向其中加入稀HNO3至酸性,滴加AgNO3溶液,若生成白色沉淀,则A中含氯原子;若生成浅黄色沉淀,则A中含溴原子,
故答案为:取反应①后的混合液少许,向其中加入稀HNO3至酸性,滴加AgNO3溶液,若生成白色沉淀,则A中含氯原子;若生成浅黄色沉淀,则A中含溴原子;
(5)符合下列条件的F( )的同分异构体:a.能发生银镜反应,说明分子中存在醛基;b.能与FeCl3溶液发生显色反应,说明分子中存在酚羟基;c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6,说明有4种氢原子,符合以上条件的F分子中有2个甲基、1个酚羟基、1个-CHO,且2个甲基处于间位,另2个分别处于对位,所以F的同分异构体有2种,为
)的同分异构体:a.能发生银镜反应,说明分子中存在醛基;b.能与FeCl3溶液发生显色反应,说明分子中存在酚羟基;c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6,说明有4种氢原子,符合以上条件的F分子中有2个甲基、1个酚羟基、1个-CHO,且2个甲基处于间位,另2个分别处于对位,所以F的同分异构体有2种,为 ,
,
故答案为:2.
点评 本题考查有机推断、有机反应类型、同分异构体、化学方程式的书写等,综合分析确定F的结构是关键,较好的考查学生分析推理能力,需要学生熟练掌握官能团的性质与转化,同分异构体的判断是易错点,难度中等.

| A. | 该实验得到的NaCl中无其他任何杂质 | |
| B. | 检验所得NaCl中是否混有BaCl2,可用AgNO3溶液检验 | |
| C. | 该实验基本操作分为溶解、过滤和蒸发三个步骤 | |
| D. | 除去杂质时,不必考虑所加试剂的顺序 |
| A. | Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | |
| B. | 用惰性电极电解CuCl2溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$4H++O2↑+2Cu | |
| C. | 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液体积混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 在酸性重铬酸钾溶液中加入少量乙醇3CH3CH2OH+2Cr2O72-+13H+→4Cr3++3CH3COO-+11H2O |
| A. | 此时溶液中NH3•H2O的物质的量浓度为$\frac{a-0.01}{2}$+10-10-10-4mol/L | |
| B. | 溶液中c(NH4+)=c(Cl-) | |
| C. | 此时水的电离程度最大 | |
| D. | 25℃时NH3•H2O的电离平衡常数Kb=$\frac{{{{10}^{-9}}}}{a-0.01}$(mol/L) |
| A. | 浓硝酸保存在棕色玻璃试剂瓶中 | |
| B. | 少量的钠保存在煤油中 | |
| C. | 氢氧化钠溶液保存在带玻璃塞的试剂瓶中 | |
| D. | 新制的氯水通常避光保存在棕色玻璃试剂瓶中 |
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为 PH3和 HI 或 H2和 I2 | |
| C. | 这种化合物能跟碱反应 | |
| D. | 该化合物可以由 PH3 和 HI 化合而成 |
| A. | 乙醇分子球棍模型: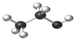 | B. | 含有10个中子的氧原子${\;}_{-8}^{-18}$O | ||
| C. | -OH的电子式: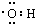 | D. | CH4Si的结构式: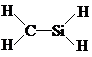 |

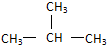
 与
与