题目内容
2.有以下各组物质,完成以下各组问题:A、O2和O3
B、${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl
C、H3CCOOC2H5与CH3COOCH3
D、CH3CH2CH2CH3与
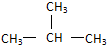
E、
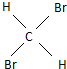 与
与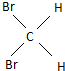
以上各组物质属于同系物的是C;属于同分异构体的是D;属于同素异形体的是A;属于同位素的是B;属于同一物质的是E.
分析 同位素:质子数相同中子数不同的同一元素的原子互称同位素;
同素异形体:同种元素组成的不同单质;
同分异构体:分子式相同结构不同的化合物;
同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的化合物;根据概念进行回答即可.
解答 解:A、O2和O3 是同种元素组成的不同单质,属于同素异形体;
B、${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl 质子数相同中子数不同,属于同位素;
C、H3CCOOC2H5与CH3COOCH3结构相似,在分子组成上相差一个或若干个CH2原子团的化合物,则属于同系物;
D、CH3CH2CH2CH3与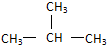 分子式相同结构不同,属于同分异构体;
分子式相同结构不同,属于同分异构体;
E、甲烷中四个氢原子是等效的, 与
与 结构相同,是同种物质.
结构相同,是同种物质.
故答案为:C;D;A;B;E.
点评 本题主要考查几同概念的辨析,注意这几种概念的要点及使用范畴是解决本题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.能说明Cl的非金属性比S的非金属性强的事实是( )
| A. | H2S的水溶液中滴加新制氯水后出现浑浊 | |
| B. | Cl原子最外层有7个电子,而S原子最外层有6个电子 | |
| C. | HCl水溶液的酸性强于H2S水溶液的酸性 | |
| D. | HClO4的酸性比H2SO3的酸性强 |
7.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1mol•L-1NaCl溶液中含有NA个Na+ | |
| B. | 25℃,101kPa,64gSO2中含有的原子数为3NA | |
| C. | 在常温常压下,22.4LCl2含有的分子数为NA | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
11.常温常压下,50mL三种气态烃的混合物与足量氧气混合点燃爆炸,恢复到原来状况时,体积共缩小100mL,则三种烃可能是( )
| A. | CH4 C2H4 C3H4 | B. | C2H6C3H6 C4H6 | C. | CH4 C2H6 C3H8 | D. | C2H4 C2H6 C3H6 |
12.500mLKNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol•L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A. | 原混合溶液中c(K+)为2mol•L-1 | B. | 上述电解过程中共转移2mol电子 | ||
| C. | 电解得到铜的物质的量为0.5mol | D. | 电解后溶液中c(H+)为2mol•L-1 |
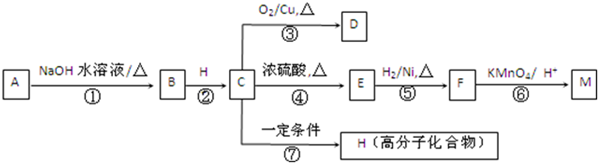
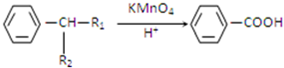 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)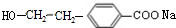 、
、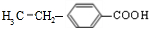 ;
; ;反应⑦的化学方程式为
;反应⑦的化学方程式为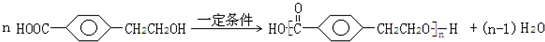 ;
; ,F1和F2互为同分异构体,G1和G2互为同分异构体. 请填空:
,F1和F2互为同分异构体,G1和G2互为同分异构体. 请填空:
 ,
, .
.