题目内容
4.2015年8月12日,天津滨海新区爆炸事故确认有氰化钠、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢气体.氰化氢的沸点只有26℃,因此相当容易挥发进入空气,这就大大增加了中毒的风险.同时氰化钠遇到亚硝酸钠会发生爆炸.回答下列问题(1)写出氰化钠遇水产生氰化氢的离子方程式CN-+H2O?HCN+OH-.
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理.氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式NaCN+H2O2+H2O═NaHCO3+NH3↑.
(3)爆炸残留在废水中的CN-可以用Cr2O72-处理,拟定下列流程进行废水处理,

1)上述处理废水流程中主要使用的方法是d;
a.混 凝法 b.中和法 c.沉淀法 d.氧化还原法
2)②中反应后无气体放出,该反应的离子方程式为CN-+ClO-═CNO-+Cl-;
3)步骤③中,每处理0.4 molCr2O72-时转移电子2.4 mol,该反应的离子方程式为3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O;
4)处理酸性Cr2O72-废水多采用铁氧磁体法.该法是向废水中加入FeSO4 •7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅡCr(2-x)Ⅲ]O4 (铁氧磁体,右上角的罗马数字表示该元素的化合价)的沉淀.处理1 mol Cr2O72-,需加入amol FeSO4 •7H2O,下列结论正确的是D.
A.x=0.5,a=6 B.x=0.5,a=10 C.x=1.5,a=6 D.x=1.5,a=10.
分析 (1)氰化钠易发生水解产生氰化氢;
(2)氰化钠与双氧水反应生成氨气和碳酸氢钠;
(3)流程分析含CN-废水调整溶液PH加入NaClO溶液,氧化CN-离子反应生成CNO-的废水,含Cr2O72-的废水调整溶液PH加入Na2S2O3发生氧化还原反应得到含硫酸根离子的废水,和含CNO-的废水继续处理得当待测水样.
1)从流程分析物质的转化关系和试剂选择分析所用方法;
2)碱性条件下,CN-离子与NaClO发生氧化还原反应生成CNO-、Cl-离子,据此写出离子方程式;
3)利用每0.4molCr2O72-转移2.4mol的电子来计算被还原后Cr元素的化合价,再书写离子方程式;
4)根据氧化还原反应中得失电子数相等,再结合原子守恒进行计算.
解答 解:(1)氰化钠易发生水解产生氰化氢,方程式为CN-+H2O?HCN+OH-,故答案为:CN-+H2O?HCN+OH-;
(2)氰化钠与双氧水反应生成氨气和碳酸氢钠,方程式为NaCN+H2O2+H2O═NaHCO3+NH3↑,故答案为:NaCN+H2O2+H2O═NaHCO3+NH3↑;
(3)流程分析含CN-废水调整溶液PH加入NaClO溶液,氧化CN-离子反应生成CNO-的废水,含Cr2O72-的废水调整溶液PH加入Na2S2O3发生氧化还原反应得到含硫酸根离子的废水,和含CNO-的废水继续处理得当待测水样.
1)从流程看,CN-转化为CNO-,化合价升高被氧化剂氧化,Cr2O72-转化为Cr3+化合价降低,故还原剂还原,故采用方法为氧化-还原法;
故答案为:d;
2)步骤②中,无气体放出,CN-被ClO-氧化为CNO-,则因为是在碱性环境中,故ClO-只能被还原为Cl-,反应式为:CN-+ClO-═CNO-+Cl-;
故答案为:CN-+ClO-═CNO-+Cl-;
3)每0.4molCr2O72-转移2.4mol的电子,设还原后Cr元素的化合价为x,则0.4mol×2×(6-x)=2.4mol,解得x=+3,则离子反应为3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O,
故答案为:3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O;
4)处理1mol Cr2O72-,需加入a mol FeSO4•7H2O,根据铬原子守恒得,1mol Cr2O72-完全反应后生成 $\frac{2}{2-x}$molFeⅡ[FeⅢx•CrⅢ2-x]O4,根据铁原子守恒得amol=$\frac{2(1+x)}{2-x}$mol①,该反应中得失电子数相等,1mol×2×3=$\frac{2}{2-x}$mol×(3-2)×x,解得x=1.5,将x=1.5代入①得a=10,
故答案为:D.
点评 本题考查物质的分离和提纯,为高频考点,涉及实验基本操作、氧化还原反应等知识点,明确流程图中化学反应原理、基本操作方法是解本题关键,难点是(4)的氧化还原反应的计算,题目难度中等.

| 实验目的 | 实验操作 | 实验原理 | |
| A | 提纯混有少量硝酸钾的氯化钠 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大 |
| B | 配制FeCl3溶液 | 将FeCl3固体溶解于适量硫酸溶液 | H+抑制FeCl3水解 |
| C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | NH3溶于水后溶质的主要存在形式是NH4+、OH- |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡 | 3Mg(OH)2+2Fe3+?2Fe(OH)3+3Mg2+ |
| A. | A | B. | B | C. | C | D. | D |
| A. | H2S的水溶液中滴加新制氯水后出现浑浊 | |
| B. | Cl原子最外层有7个电子,而S原子最外层有6个电子 | |
| C. | HCl水溶液的酸性强于H2S水溶液的酸性 | |
| D. | HClO4的酸性比H2SO3的酸性强 |

| A. | Al和Fe2O3的铝热反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | NaOH溶液与CH3COOH溶液反应 | D. | 甲烷在O2中的燃烧反应 |
| A. | 天然气、酒精和汽油分别属于化石能源、可再生能源和二次能源 | |
| B. | 富含N、P元素的生活用水可以直接用来灌溉农田 | |
| C. | 液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性 | |
| D. | 我国油品从国 IV 汽油升级到国 V 汽油,有助于减少酸雨、雾霾,提高空气质量 |
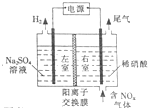 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
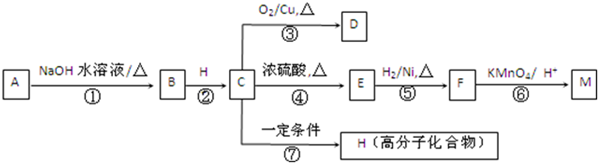
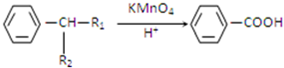 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)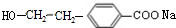 、
、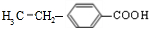 ;
; ;反应⑦的化学方程式为
;反应⑦的化学方程式为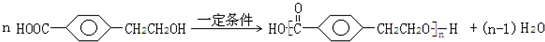 ;
;