题目内容
5.从某微粒的原子结构示意图反映出( )| A. | 质子数和中子数 | |
| B. | 核电荷数和核外电子层排布的电子数 | |
| C. | 中子数和电子数 | |
| D. | 质量数和核外电子层排布的电子数 |
分析 原子结构示意图是表示原子核电荷数和电子层排布的图示形式,而中子数和质量数没有体现,据此进行判断.
解答 解:A.在微粒的原子结构示意图上,只能体现出原子核电荷数和电子层排布的图示形式,中子数没有体现,故A错误;
B.原子结构示意图是表示原子核电荷数和电子层排布的图示形式,能反映出核电荷数和核外电子层排布的,故B正确;
C.在微粒的原子结构示意图上,只能体现出原子核电荷数和电子层排布的图示形式,中子数没有体现,故C错误;
D.在微粒的原子结构示意图上,只能体现出原子核电荷数和电子层排布的图示形式,质量数数没有体现,故D错误;
故选B.
点评 本题考查了原子结构示意图表示的意义,题目难度不大,明确原子结构示意图的表示方法为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
16.下列反应的离子方程式正确的是( )
| A. | 向NaOH溶液中加入铝粉来制备H2:Al+2OH-+2H2O═AlO2-+3H2↑ | |
| B. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 实验室用氢氧化钠溶液吸收Cl2:Cl2+OH-═Cl-+ClO-+H2O | |
| D. | 用胃舒平治疗胃酸过多:Al(OH)3+3H+═Al3++3H2O |
20.下列半径比较正确的是( )
| A. | Na、Mg、Ca原子半径从大到小 | B. | O2-、Na+、K+半径从小到大 | ||
| C. | Cl、Cl- 半径前者大 | D. | H、N、Al 半径从小到大 |
10.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | 氢化物的沸点为H2T<H2X | |
| B. | R的氧化物对应的水化物可能具有两性 | |
| C. | X单质在氧气中燃烧生成XO3 | |
| D. | L、X形成的简单离子核外电子数相等 |
14.下列实验能达到目的是( )
| A. | 将NH4Cl溶液蒸干灼烧制备NH4Cl固体 | |
| B. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| C. | 用可见光束照射以区别溶液和胶体 | |
| D. | 用分液的方法分离酒精和水的混合物 |
15.下列有关化学用语的表示方法中正确的是( )
| A. | H2O2的电子式: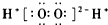 | |
| B. | CO2分子的结构式:O═C═O | |
| C. | 原子核内有8个中子的碳原子:${\;}_8^{14}C$ | |
| D. | 氯化钾的分子式:KCl |