题目内容
20.对于相同体积的K2CO3溶液(浓度为c1)和溶液(NH4)2CO3(浓度为c2),若其中CO32-的物质的量浓度相同,则c1和c2的关系是( )| A. | c1=2c2 | B. | c1>c2 | C. | c1=c2 | D. | c1<c2 |
分析 (NH4)2CO3是弱酸弱碱盐,发生相互促进的水解;碳酸钾中碳酸根离子的水解不受影响,由此分析解答;
解答 解:K2CO3是易溶于水的盐,在水中完全电离,电离出的碳酸根离子部分水解,但水解微弱,(NH4)2CO3是易溶于水的盐,在水中完全电离,电离出的铵根离子和碳酸根离子分别和水电离出的氢氧根离子和氢离子结合,水解相互促进,所以,碳酸根离子浓度比K2CO3中碳酸根离子离子浓度小一些,若二者中CO32-的物质的量浓度相同,则碳酸铵的浓度大.
故选D.
点评 本题主要考查了盐类水解的应用,解答须掌握盐类水解的规律影响因素及应用,难度中等.

练习册系列答案
相关题目
17.下列各组离子一定能大量共存的是( )
| A. | 在含有大量 Al3+的无色溶液中:Cu2+、Na+、Cl-、SO 42- | |
| B. | 在含有大量 H+的 溶液中:Na+、K+、CO 32-、NO3- | |
| C. | 在强酸的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | 在滴加石蕊显蓝色的溶液中:K+、Cu2+、Cl-、NO2- |
15.一定温度下,石灰乳悬浊液中存在下列平衡:Ca(OH)2(s)?Ca2+(aq)+2OH?(aq)下列说法正确的是( )
| A. | 恒温下向溶液中加入CaO,Ca2+离子数目减少 | |
| B. | 恒温下向溶液中加入CaO,溶液中C(Ca2+)减小 | |
| C. | 给溶液加热,溶液的pH不变 | |
| D. | 给溶液加热,溶液的离子浓度增大 |
12.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A. | 常温下,48gO3含有的氧原子数3NA | |
| B. | 33.6LCO中含有的原子数是3NA | |
| C. | 0.5mol•L-1CaCl2溶液中含Cl-数目为NA | |
| D. | 17gNH3所含的电子数为10NA |
9.将10mL充满NO2和O2混合气体的试管倒立在水槽中,反应停止后试管剩余2mL无色气体,原混合气体中NO2和O2各是多少毫升( )
| A. | 8.2mL和1.8mL | B. | 5.6mL和4.4mL | C. | 6.4mL和3.6mL | D. | 3.5mL和6.5mL |
10.下列说法正确的是( )
| A. | 具有相同质子数的微粒一定属于同一种元素 | |
| B. | H2O和H2O2互为同素异形体 | |
| C. | 含有金属元素的离子不一定是阳离子 | |
| D. | 同种元素的原子中,中子数和质子数一定都相同 |
 某化学创新实验小组设计如图示实验装置来制取溴苯并证明该反应为取代反应.已知:溴苯的熔点为?30.8℃,沸点156℃.
某化学创新实验小组设计如图示实验装置来制取溴苯并证明该反应为取代反应.已知:溴苯的熔点为?30.8℃,沸点156℃.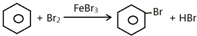 ;
;