题目内容
12.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )| A. | 常温下,48gO3含有的氧原子数3NA | |
| B. | 33.6LCO中含有的原子数是3NA | |
| C. | 0.5mol•L-1CaCl2溶液中含Cl-数目为NA | |
| D. | 17gNH3所含的电子数为10NA |
分析 A.氧元素守恒计算物质的量n=$\frac{m}{M}$,得到微粒数;
B.标准状况下气体摩尔体积为22.4L/mol;
C.溶液体积不知不能计算微粒数;
D.物质的量n=$\frac{m}{M}$,氨气分子中含10个电子.
解答 解:A.常温常压下,48g O3含有的氧原子数为:$\frac{48g}{16g/mol}$×NA=3mol×NA=3NA,故A正确;
B.温度压强不知,33.6LCO物质的量不能计算,故B错误;
C.0.5mol•L-1CaCl2溶液中含Cl-浓度为1mol/L,体积不知不能计算氯离子微粒数,故C错误;
D.17gNH3的物质的量=$\frac{17g}{17g/mol}$=1mol,所含的电子数为10NA ,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是物质的量和微粒数计算关系、气体摩尔体积条件应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
9.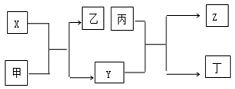 由短周期主族元素X、Y、Z组成的单质(化学式也分别为X、Y、Z),X为金属,其核外电子数为Y原子序数的2倍,Y的最低负化合价与Z的最高正化合价的数值相等,甲、乙、丙、丁四种均为氧化物,甲和丁为无色的气体,固体甲可用于人工降雨,乙和丙熔点均很高,且它们在一定条件下能发生如下反应,下列说法中正确的是( )
由短周期主族元素X、Y、Z组成的单质(化学式也分别为X、Y、Z),X为金属,其核外电子数为Y原子序数的2倍,Y的最低负化合价与Z的最高正化合价的数值相等,甲、乙、丙、丁四种均为氧化物,甲和丁为无色的气体,固体甲可用于人工降雨,乙和丙熔点均很高,且它们在一定条件下能发生如下反应,下列说法中正确的是( )
 由短周期主族元素X、Y、Z组成的单质(化学式也分别为X、Y、Z),X为金属,其核外电子数为Y原子序数的2倍,Y的最低负化合价与Z的最高正化合价的数值相等,甲、乙、丙、丁四种均为氧化物,甲和丁为无色的气体,固体甲可用于人工降雨,乙和丙熔点均很高,且它们在一定条件下能发生如下反应,下列说法中正确的是( )
由短周期主族元素X、Y、Z组成的单质(化学式也分别为X、Y、Z),X为金属,其核外电子数为Y原子序数的2倍,Y的最低负化合价与Z的最高正化合价的数值相等,甲、乙、丙、丁四种均为氧化物,甲和丁为无色的气体,固体甲可用于人工降雨,乙和丙熔点均很高,且它们在一定条件下能发生如下反应,下列说法中正确的是( )| A. | X为第三周期II族元素,Y和Z位于同一主族 | |
| B. | 甲、乙、丙均能与水发生化合反应 | |
| C. | 工业上常用电解乙制备X | |
| D. | X可用于制焰火烟花,Z可用作太阳能电池的材料 |
20.对于相同体积的K2CO3溶液(浓度为c1)和溶液(NH4)2CO3(浓度为c2),若其中CO32-的物质的量浓度相同,则c1和c2的关系是( )
| A. | c1=2c2 | B. | c1>c2 | C. | c1=c2 | D. | c1<c2 |
7.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 淀粉溶液、豆浆、碳素墨水均可发生丁达尔现象 | |
| B. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 | |
| C. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| D. | 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯 |
17.完全中和一定量的H2SO4溶液用去NaOH 4g.若改用KOH中和,则需要KOH( )
| A. | 0.2 mol | B. | 0.14mol | C. | 4g | D. | 5.6g |
4.取10g粗铁加入足量稀硫酸中,共收集到5.6L氢气(标准状况),则粗铁中混有的杂质不可能是( )
| A. | Cu和Mg | B. | Mg和Al | C. | Al 和 Si | D. | SiO2和Zn |
2.下列对化学用语的理解正确的是( )
| A. | 离子结构示意图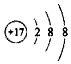 ,可以表示35Cl-,也可以表示37Cl- ,可以表示35Cl-,也可以表示37Cl- | |
| B. | 电子式 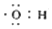 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| C. | 比例模型 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 聚丙烯的结构简式为: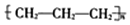 |