题目内容
5.观察如图所示装置,回答下列问题: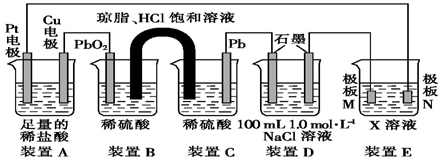
(1)装置B中PbO2上发生的电极反应为PbO2+2e-+4H++SO42-═PbSO4+2H2O
(2)装置A中总反应的离子方程式为Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑.
(3)若装置E的目的是在Cu上镀Ag,则X为AgNO3,极板N的材料为Ag.
(4)当装置A中Cu电极的质量改变了6.4g时,写出装置D中阳极的电极反应式2Cl-2e-=Cl2↑、4OH-4e-=2H2O+O2↑ 装置D中产生的气体体积为3.92L(标准状况下).
分析 (1)B和C装置形成原电池,铅作负极,二氧化铅作正极,正极上二氧化铅得电子和硫酸根离子反应生成硫酸铅;
(2)A为电解装置,铜为阳极,阴极生成氢气;
(3)电镀时,镀层作阳极,镀件作阴极,电解质溶液中阳离子和镀层金属相同;
(4)根据转移电子守恒计算生成气体的体积.
解答 解:(1)B和C装置形成原电池,铅作负极,二氧化铅作正极,原电池放电时,正极上二氧化铅得电子和硫酸根离子反应生成硫酸铅,发生还原反应,电极反应式为:PbO2+2e-+4H++SO42-═PbSO4+2H2O,故答案为:PbO2+2e-+4H++SO42-═PbSO4+2H2O;
(2)A为电解装置,铜为阳极,阴极生成氢气,电解方程式为Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑,故答案为:Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑;
(3)电镀时,镀层作阳极,镀件作阴极,电解质溶液中阳离子和镀层金属相同,若装置D的目的是在某镀件上镀银,则X为硝酸银溶液,N作阳极,应该是银,若装置E的目的是验证金属的电化学防腐,则极板N的材料为惰性电极(或石墨等不溶性惰性材料),被保护的金属连接电源阴极,
故答案为:AgNO3;Ag;
(4)当装置A中Cu电极质量改变6.4g时,n(Cu)=0.1mol,则转移0.2mol电子,装置D中n(NaCl)=0.1mol,
阳极首先发生2Cl-2e-=Cl2↑、其次发生4OH-4e-=2H2O+O2↑,则阳极首先生成0.05molCl2,其次生成0.025molO2,
阴极只发生2H++2e-=H2↑,生成0.1molH2,则总共生成0.175mol气体,体积为0.175mol×22.4L/mol=3.92L,
故答案为:2Cl-2e-=Cl2↑、4OH-4e-=2H2O+O2↑;3.92.
点评 本题考查了原电池和电解池原理,为高频考点,侧重于学生的分析能力和计算能力的考查,明确离子放电顺序是解本题关键,难点是电极反应式的书写,难度中等.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 磷酸与烧碱、硝酸与澄淸石灰水 | |
| B. | 氯化钡与硫酸钠、硫酸与硝酸钡 | |
| C. | 碳酸铵与氢氧化钠、碳酸铵与石灰乳 | |
| D. | 纯碱与硫酸、碳酸氢钾与盐酸 |
| A. | AgCl>AgI>AgBr | B. | AgCl>AgBr>AgI | C. | AgBr>AgCl>AgI | D. | AgBr>AgI>AgCl |
| A. | c1=2c2 | B. | c1>c2 | C. | c1=c2 | D. | c1<c2 |
| A. | 1:1 | B. | 5:3 | C. | 33:11 | D. | 11:4 |
| A. | 0.2 mol | B. | 0.14mol | C. | 4g | D. | 5.6g |
| A. | NaOH | B. | NH4Cl | C. | CH3COONa | D. | HC1 |