题目内容
W克下列物质电火花引燃后的产物通过足量的Na2O2后,固体增重大于W克的是( )
| A、CO与H2的混合气体 |
| B、CH3CH2OH |
| C、HCOOH |
| D、CH3COOH |
考点:化学方程式的有关计算
专题:计算题
分析:H2、CO在整个过程中发生的化学方程式为:2H2+O2
2H2O、2Na2O2+2H2O=4NaOH+O2↑;2CO+O2
2CO2、2Na2O2+2CO2=2Na2 CO3+O2,由反应方程式可知,过氧化钠增加的质量即为H2、CO的质量.因此只要是CO或H2或它们的混合气体或化学组成符合(CO)m?(H2)n,固体增重等于W克,不符合此CO)m?(H2)n形式的,多O的增重的质量小于ag,多C的增重的质量大于ag,满足题意.
| ||
| ||
解答:
解:A.H2、CO在整个过程中发生的化学方程式为:2H2+O2
2H2O、2Na2O2+2H2O=4NaOH+O2↑;2CO+O2
2CO2、2Na2O2+2CO2=2Na2CO3+O2,由反应方程式可知,过氧化钠增加的质量即为H2、CO的质量,所以固体增重等于W克,故A错误;
B.乙醇CH3CH2OH可表示为(CO)1?(H2)3?C,固体增重大于W克,故B正确;
C.甲酸HCOOH,可以写成CO1(H2)?O,固体质量增加小于W克,故C错误;
D.CH3COOH可表示为(CO)2?(H2)2,固体增重等于W克,故D错误;
故选B.
| ||
| ||
B.乙醇CH3CH2OH可表示为(CO)1?(H2)3?C,固体增重大于W克,故B正确;
C.甲酸HCOOH,可以写成CO1(H2)?O,固体质量增加小于W克,故C错误;
D.CH3COOH可表示为(CO)2?(H2)2,固体增重等于W克,故D错误;
故选B.
点评:本题考查化学方程式的有关计算,注意根据方程式利用差量法进行解答,侧重考查学生分析解决问题的能力,题目难度中等.

练习册系列答案
相关题目
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0g,若上述气体为NO和NO2的混合物,且体积比为1:1,则v可能为( )
| A、9.0L | B、13.5L |
| C、10.7L | D、16.8L |
下列有关环境保护的说法中正确的是( )
| A、含氮、磷化合物的生活污水大量排放可使水体富营养化,造成潮汐 |
| B、各国工业大量排放二氧化硫是全球气候变暖的主要原因 |
| C、劣质装修材料中的甲醛、苯、氡气等对人体有害 |
| D、废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染 |
室温下,将1mol的CuSO4?5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2;CuSO4?5H2O受热分解的化学方程式为:CuSO4?5H2O(s)
CuSO4(s)+5H2O(l),热效应为△H3.则下列判断正确的是( )
| ||
| A、△H2>△H3 |
| B、△H1<△H3 |
| C、△H1+△H3=△H2 |
| D、△H1+△H2=△H3 |
下列实验中所选用的仪器合理的是( )
| A、用200mL量筒量取5.2mL稀硫酸 |
| B、用碱式滴定管量取22.10mL溴水 |
| C、用托盘天平称取11.70g食盐 |
| D、用250mL容量瓶配制230mL0.2 mol?L-1的氢氧化钠溶液 |
将3.2g硫粉和16.8g铁粉混合均匀后放入试管里加热,充分反应,冷却,再加入足量稀硫酸,产生的气体体积(S.T.P)是( )
| A、6.72 L |
| B、3.36 L |
| C、2.24 L |
| D、以上都不对 |
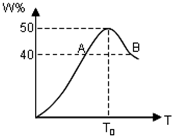 2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线:
2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线: