题目内容
13.某温度下,反应N2O4(g)?2NO2(g),△H>0,在体积可变的密闭容器中达到平衡.下列说法正确的是( )| A. | 保持温度和体积不变,加入少许N2O4,再达到平衡时,颜色变深 | |
| B. | 保持温度和体积不变,加入少许NO2,将使正反应速率减小 | |
| C. | 保持温度不变,增大压强时,将使正反应速率增大,逆反应速率减小 | |
| D. | 保持体积不变,升高温度,再达平衡时颜色变浅 |
分析 增大浓度、压强,反应速率均增大,该反应为吸热反应,升高温度平衡正向移动,以此来解答.
解答 解:A.保持温度和体积不变,加入少许N2O4,再达到平衡时,NO2的浓度比原平衡时浓度大,则颜色变深,故A正确;
B.保持温度和体积不变,加入少许NO2,生成物浓度增大,将使正反应速率比原平衡时速率大,故B错误;
C.保持温度不变,增大压强时,将使正反应速率、逆反应速率均增大,故C错误;
D.该反应为吸热反应,保持体积不变,升高温度,平衡正向移动,再达平衡时颜色变深,故D错误;
故选A.
点评 本题考查化学平衡的影响因素,为高频考点,把握温度、浓度、压强对反应速率及平衡的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
3.C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元素周期表第三周期第IVA族.
(2)N的基态原子核外电子排布式为1s22s22p3. Cu的基态原子最外层有1个电子.
(3)用“>”或“<”填空:
(1)Si位于元素周期表第三周期第IVA族.
(2)N的基态原子核外电子排布式为1s22s22p3. Cu的基态原子最外层有1个电子.
(3)用“>”或“<”填空:
| 原子半径 | 电负性 |
| Al>Si | N<O |
1.下列实验能达到预期目的是( )
①用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
②用溴水除去乙烷中混有的乙烯
③用氢气通过加成反应除去乙烷中混有的乙烯
④用苯的邻二氯代物只有一种证明苯的碳碳键完全相同.
①用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
②用溴水除去乙烷中混有的乙烯
③用氢气通过加成反应除去乙烷中混有的乙烯
④用苯的邻二氯代物只有一种证明苯的碳碳键完全相同.
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |

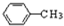 .
. .
.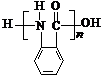 的单体.
的单体.
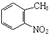 ,试剂a为酸性高锰酸钾溶液.
,试剂a为酸性高锰酸钾溶液.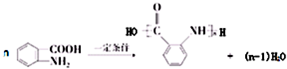 .
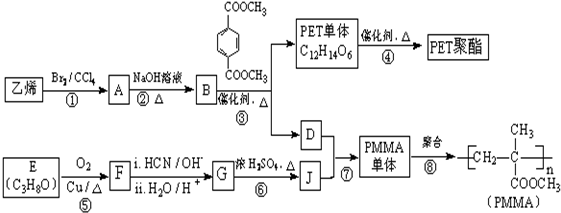
.
 $→_{H_{2}O/H+}^{i.HCN/OH-}$
$→_{H_{2}O/H+}^{i.HCN/OH-}$ (R、R′代表烃基)
(R、R′代表烃基)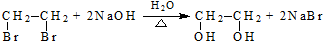
 .
.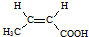 .
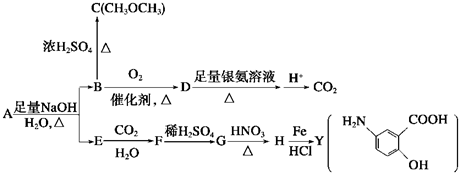
.
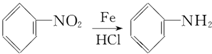
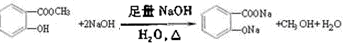 .
.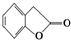 和
和 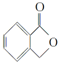 ,鉴别I和J的试剂为FeCl3或浓溴水.
,鉴别I和J的试剂为FeCl3或浓溴水.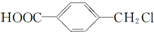 制得,写出K在浓硫酸作用下生成的聚合物的结构简式:
制得,写出K在浓硫酸作用下生成的聚合物的结构简式: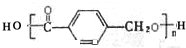 .
.