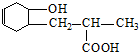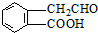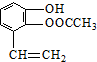题目内容
20.将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.由此可见( )| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O△H>0 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 该反应中,反应物吸收环境中的热量转化为产物内部的能量 |
分析 醋酸逐渐凝固说明反应吸收热量导致醋酸溶液温度降低,即NH4HCO3与HCl的反应为吸热反应,说明反应物的总能量小于生成物的总能量,以此解答该题.
解答 解:A.醋酸逐渐凝固说明反应吸收热量导致醋酸溶液温度降低,即NH4HCO3与HCl的反应为吸热反应,故A错误;
B.书写热化学方程式时,应注明物质的状态,故B错误;
C.因反应为吸热反应,则反应后生成物的总能量高于反应物的总能量,故C错误;
D.因反应为吸热反应,即吸热的热量转化为产物内部的能量,故D正确.
故选D.
点评 本题考查化学反应能量变化判断,为高频考点,侧重于学生的分析能力的考查,注意热化学方程式书写方法,题目难度中等.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
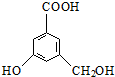
11.有机化合物A(C9H10O2)为一种无色液体.从A出发可发生如图的一系列反应.则下列说法正确的是( )


| A. | 根据图示可推知D为苯酚 | |
| B. | G的同分异构体中属于酯且能发生银镜反应的只有两种 | |
| C. | 上述各物质中能发生水解反应的有A、B、D、G | |
| D. | A的结构中含有碳碳双键 |
15.下列叙述错误的是( )
| A. | 工业上,乙苯主要通过苯与乙烯在合适条件下加成反应获得 | |
| B. | 实验室制得的溴苯含有多种有机杂质,除了苯之外,还可能含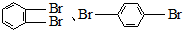 | |
| C. | 萘(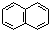 )不是苯的同系物,应属于联苯类芳香烃 )不是苯的同系物,应属于联苯类芳香烃 | |
| D. | D.甲苯与氯气在光照下反应生成的一氯代物主要为 |
5.已知:P4(g)+6Cl2(g)=4PCl3(g).1mol P4(g)与氯气完全反应生成PCl3(g)放出a kJ的热量,P4具有正四面体结构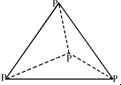 ,打破1mol P-Cl键吸收b kJ的热量,打破1mol Cl-Cl键吸收c kJ的热量.下列叙述正确的是( )
,打破1mol P-Cl键吸收b kJ的热量,打破1mol Cl-Cl键吸收c kJ的热量.下列叙述正确的是( )
 ,打破1mol P-Cl键吸收b kJ的热量,打破1mol Cl-Cl键吸收c kJ的热量.下列叙述正确的是( )
,打破1mol P-Cl键吸收b kJ的热量,打破1mol Cl-Cl键吸收c kJ的热量.下列叙述正确的是( )| A. | 1 mol P4(g)和1 mol Cl2(g)所具有的能量和大于1 mol PCl3(g) 所具有的能量 | |
| B. | 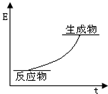 该反应的能量图象可表示 该反应的能量图象可表示 | |
| C. | 形成1mol P-P键放出-($\frac{a}{6}$-2b+c) kJ的热量 | |
| D. | 因为该反应为放热反应,故不需要任何条件就能快速进行 |
12.同周期的X、Y、Z三种元素,已知其高价氧化物对应的水化物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中正确的是( )
| A. | 原子半径:X>Y>Z | B. | 原子序数:X<Y<Z | ||
| C. | 气态氢化物稳定性:X<Y<Z | D. | 非金属性:X>Y>Z |
9.下列关于有机物结构、性质的说法正确的是( )
| A. | 石油裂解的主要目的是提高汽油等轻质油的产量与质量,石油催化裂化的主要目的是得到更多的乙烯、丙烯等气态短链烃 | |
| B. | 分子式为C3H7C1的有机物有三种同分异构体 | |
| C. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 | |
| D. | 向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
 ;
;