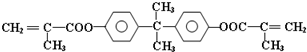
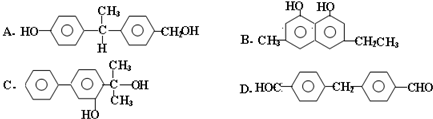
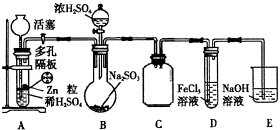
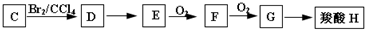题目内容
12.同周期的X、Y、Z三种元素,已知其高价氧化物对应的水化物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中正确的是( )| A. | 原子半径:X>Y>Z | B. | 原子序数:X<Y<Z | ||
| C. | 气态氢化物稳定性:X<Y<Z | D. | 非金属性:X>Y>Z |
分析 同周期自左而右元素非金属性增强,非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,原子序数:X>Y>Z;同周期元素的原子从左到右,原子半径逐渐减小、氢化物的稳定性逐渐增强,以此解答该题.
解答 解:同周期自左而右元素非金属性增强,非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,原子序数:X>Y>Z;同周期元素的原子从左到右,原子半径逐渐减小、氢化物的稳定性逐渐增强.
A.同周期从左到右非金属性增强,原子半径逐渐减小,所以原子半径:X<Y<Z,故A错误;
B.非金属性X>Y>Z,同周期从左到右元素非金属性增强,可知原子序数的关系为X>Y>Z,故B错误;
C.非金属性越强,氢化物越稳定,由于非金属性X>Y>Z,所以气态氢化物的稳定性:HX>H2Y>ZH3,故C错误;
D.最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,故D正确.
故选D.
点评 本题考查元素周期律知识,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意相关性质的比较角度以及元素周期律的主要递变规律.

练习册系列答案
相关题目
2.对下列事实的解释正确的是( )
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 | |
| B. | 向某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,则原溶液一定含有SO42- | |
| C. | 常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化 | |
| D. | 浓硝酸在光照下变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 |
20.将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.由此可见( )
| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O△H>0 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 该反应中,反应物吸收环境中的热量转化为产物内部的能量 |
7.为回收利用废钒催化剂(含有V2O5,、及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如图1:
已知部分含钒物质在水中的溶解性如下:
回答下列问靥:
(1)工业由V2O5冶炼金厲钒常用铝热法,写出该反应的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(2)滤液中含钒的主要成分为VOSO4 (写化学式).
(3)反应③的沉淀率是回收钒的关键,该步反应的离子方程式为NH4++VO3-=NH4VO3↓;沉淀率的髙
低除受溶液pH影响外,还与氯化按系数(NH4Cl加入质量与样品中V2O5的质量比)和温度有关.根据图2判断最佳氯化铵系数和温度分别为4、80°C.
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,该滴定反应的离子方程式2VO2++H2C2O4+2H+═2VOn++2CO2↑+2H2O.若产生2.24L的CO2(标准状况下),则转移电子数为0.1NA.
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:VO${\;}_{2}^{+}$+V2++H+ $?_{放电}^{充电}$ VO2++H2O+V3+
电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+.
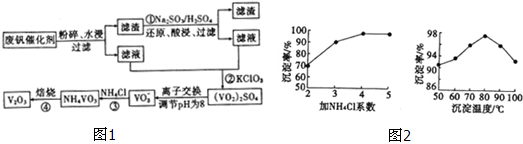
已知部分含钒物质在水中的溶解性如下:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
(1)工业由V2O5冶炼金厲钒常用铝热法,写出该反应的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(2)滤液中含钒的主要成分为VOSO4 (写化学式).
(3)反应③的沉淀率是回收钒的关键,该步反应的离子方程式为NH4++VO3-=NH4VO3↓;沉淀率的髙
低除受溶液pH影响外,还与氯化按系数(NH4Cl加入质量与样品中V2O5的质量比)和温度有关.根据图2判断最佳氯化铵系数和温度分别为4、80°C.
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,该滴定反应的离子方程式2VO2++H2C2O4+2H+═2VOn++2CO2↑+2H2O.若产生2.24L的CO2(标准状况下),则转移电子数为0.1NA.
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:VO${\;}_{2}^{+}$+V2++H+ $?_{放电}^{充电}$ VO2++H2O+V3+
电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+.

17.下列关于元素周期表的说法正确的是( )
| A. | 每一周期的元素都从碱金属开始,最后以稀有气体结束 | |
| B. | 第二、三周期上下相邻的元素的原子核外电子数相差8个 | |
| C. | 只有第2列元素的原子最外层有2个电子 | |
| D. | 元素周期表共有十六个纵行,也就是十六个族 |
4.下列叙述从化学角度分析,其中正确的是( )
| A. | 相同物质的量的烃,完全燃烧,生成的CO2越多,说明烃中的碳的质量分数越大 | |
| B. | 相同质量的烃,完全燃烧,消耗的O2越多,说明烃中的氢的质量分数越大 | |
| C. | 银镜反应实验后试管内壁附有银,可用氨水清洗 | |
| D. | 氟利昂(CF2Cl2)或氮氧化物(NOx)气体会破坏大气臭氧层,从而导致“温室效应” |
1.下列说法正确的是( )
| A. | 反应热就是反应中放出的能量 | |
| B. | 在101 kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少 | |
| D. | 由C(石墨)═C(金刚石)△H=+1.9 kJ•mol-1可知,石墨稳定 |