题目内容
书写下列物质的电离方程式
(1)H2SO4
(2)Ba(OH)2
(3)CH3COOH
(4)NH3?H2O .
(1)H2SO4
(2)Ba(OH)2
(3)CH3COOH
(4)NH3?H2O
考点:电离方程式的书写
专题:离子反应专题
分析:(1)硫酸为二元强酸,完全电离出氢离子和硫酸根离子,硫酸根离子团在电离方程式中不能再拆;
(2)氢氧化钡为二元强碱,完全电离出钡离子和氢氧根离子;
(3)CH3COOH是弱电解质,在水溶液里部分电离出乙酸根离子与氢离子;
(4)一水合氨为弱电解质,部分电离出铵根离子和氢氧根离子.
(2)氢氧化钡为二元强碱,完全电离出钡离子和氢氧根离子;
(3)CH3COOH是弱电解质,在水溶液里部分电离出乙酸根离子与氢离子;
(4)一水合氨为弱电解质,部分电离出铵根离子和氢氧根离子.
解答:
解:(1)硫酸为二元强酸,完全一步电离出氢离子和硫酸根离子,电离方程式为:H2SO4=2H++SO42-,故答案为:H2SO4=2H++SO42-;
(2)氢氧化钡为二元强碱,完全一步电离出钡离子和氢氧根离子,电离方程式为:Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-;
(3)乙酸是弱电解质,在水溶液里部分电离,电离方程式为:CH3COOH?H++CH3COO-,故答案为:CH3COOH?H++CH3COO-;
(4)氨水是一元弱碱,部分电离出铵根离子和氢氧根离子,电离方程式为:NH3?H2O?NH4++OH-,故答案为:NH3?H2O?NH4++OH-.
(2)氢氧化钡为二元强碱,完全一步电离出钡离子和氢氧根离子,电离方程式为:Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-;
(3)乙酸是弱电解质,在水溶液里部分电离,电离方程式为:CH3COOH?H++CH3COO-,故答案为:CH3COOH?H++CH3COO-;
(4)氨水是一元弱碱,部分电离出铵根离子和氢氧根离子,电离方程式为:NH3?H2O?NH4++OH-,故答案为:NH3?H2O?NH4++OH-.
点评:本题考查了电离方程式的书写,题目难度不大,注意掌握电离方程式的书写原则,注意掌握强弱电解质的区别,注意强电解质与弱电解质的电离方程式的书写方法.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
镍铬(Ni-Cd)可充电电池的电解质溶液为KOH溶液,它的充、放电反应按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和NiOOH都不溶于KOH溶液.则下列说法正确的是( )
| 放电 |
| 充电 |
| A、放电时负极:Cd-2e-═Cd2+ |
| B、放电时正极区碱性增强 |
| C、充电时阳极:2Ni(OH)2-2e-+4H+═2Ni3++4H2O |
| D、充电时阴极:电极发生还原反应,电极质量增大 |
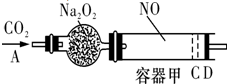 如图装置中,容器甲内充入1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时,容器体积缩小至最小,为原体积的
如图装置中,容器甲内充入1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时,容器体积缩小至最小,为原体积的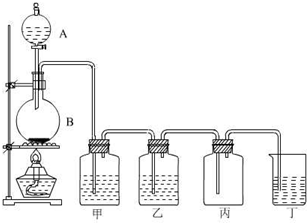
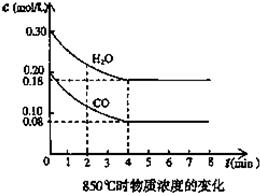 在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)?CO2(g)十H2 (g)△H=Q KJ?mol-1 (Q>0)CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=
在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)?CO2(g)十H2 (g)△H=Q KJ?mol-1 (Q>0)CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=