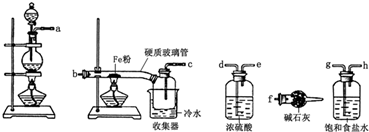
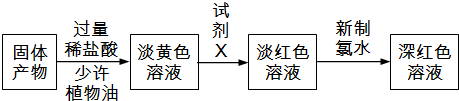
��Ŀ����
2014��12���ҹ���������������﮵�ض��������Ϻ�˳����ˮ���ҹ��Ĵ��������ѽ���һ��ո�µ�ʱ�����ɼ����о���ѧ��Ӧԭ���зdz���Ҫ�����壮
��1��������﮵����������ﮣ�LiFePO4��Ϊ�������ϵ�����ӵ�أ�
��֪������ӵ�ص��ܷ�ӦΪLi1-xFePO4+LixC6
6C+LiFePO4��Li1-xFePO4��LixC6��LiΪ����״̬������õ�طŵ�ʱ�����ĵ缫��ӦʽΪ ���Ըõ��Ϊ��Դ����ͭΪ��������ʯīΪ��������NaCl��Һ�����Һ���е�⣬�õ��뵼�����Cu2O��һ�������Դ����������ӦʽΪ ��
��2��25��ʱ�����ֵ���ʵĵ���ƽ�ⳣ�����±���ʾ��
��25�棬0.1mol?L-1HF��Һ��H+Ũ��Ϊ mol?L-1��100mL 0.1mol?L-1NaF��Һ�������������� ���������������=����100mL 0.1mol?L-1CH3COONa��Һ����������������
����10mL0.1mol?L-1CH3COOH��Һ����εμ�0.1mol?L-1�İ�ˮ�������İ�ˮ10mLʱ��Һ�и�����Ũ�ȵĴ�С��ϵ�� ��
����֪NaH2PO4��Һ�����Զ�Na2HPO4��Һ�Լ��ԣ�25�棬Ũ�Ⱦ�Ϊ0.1mol?L-1 NaH2PO4��Na2HPO4��Һ��ˮ�ĵ���̶� ���ǰ�ߴ������ߴ���ȡ�����
��1��������﮵����������ﮣ�LiFePO4��Ϊ�������ϵ�����ӵ�أ�
��֪������ӵ�ص��ܷ�ӦΪLi1-xFePO4+LixC6
| �ŵ� |
| ��� |
��2��25��ʱ�����ֵ���ʵĵ���ƽ�ⳣ�����±���ʾ��
| ����� | ���볣����mol?L-1�� |
| H3PO4 | Ka1=7.1��10-3��Ka2=6.2��10-8��Ka3=4.5��10-13 |
| HF | Ka=6.4��10-4 |
| CH3COOH | Ka=1.7��10-5 |
| NH3?H2O | Kb=1.7��10-5 |
����10mL0.1mol?L-1CH3COOH��Һ����εμ�0.1mol?L-1�İ�ˮ�������İ�ˮ10mLʱ��Һ�и�����Ũ�ȵĴ�С��ϵ��
����֪NaH2PO4��Һ�����Զ�Na2HPO4��Һ�Լ��ԣ�25�棬Ũ�Ⱦ�Ϊ0.1mol?L-1 NaH2PO4��Na2HPO4��Һ��ˮ�ĵ���̶�
���㣺���������ˮ��Һ�еĵ���ƽ��,ԭ��غ͵��صĹ���ԭ��
ר�⣺
��������1��ԭ��ص������Ϸ����õ��ӵĻ�ԭ��Ӧ���ڵ��ص������Ϸ���ʧ���ӵ�������Ӧ��
��2���ٸ���Ka=
�����㼴�ɣ��ε�ˮ����ɣ�Խ��Խˮ�⣻
�ڸ��ݷ�Ӧ�õ�����Һ����ɽ����Һ������Խ����ж�����Ũ�ȵĴ�С���ɣ�
�۸���NaH2PO4��Һ�����Զ�Na2HPO4��Һ�Լ��ԣ��õ������ӵ�ˮ��̶Ⱥ͵���̶ȵ���Դ�С��ˮ���ˮ�ĵ����ٽ����ã������ˮ�ĵ������������ã�
��2���ٸ���Ka=
| c(H+)?c(F-) |
| c(HF) |
�ڸ��ݷ�Ӧ�õ�����Һ����ɽ����Һ������Խ����ж�����Ũ�ȵĴ�С���ɣ�
�۸���NaH2PO4��Һ�����Զ�Na2HPO4��Һ�Լ��ԣ��õ������ӵ�ˮ��̶Ⱥ͵���̶ȵ���Դ�С��ˮ���ˮ�ĵ����ٽ����ã������ˮ�ĵ������������ã�
���
�⣺��1������ӵ�ص��ܷ�ӦΪLi1-xFePO4+LixC6
6C+LiFePO4��Li1-xFePO4��LixC6��LiΪ����״̬������õ�طŵ�ʱ�����Ϸ����õ��ӵĻ�ԭ��Ӧ�����缫��ӦʽΪFePO4+Li++e-��LiFePO4���Ըõ��Ϊ��Դ����ͭΪ��������ʯīΪ��������NaCl��Һ�����Һ���е�⣬�õ��뵼�����Cu2O��һ�������Դ���������ǽ���ͭʧ���ӵ�������Ӧ����ӦʽΪ2Cu+2H2O-2e-=Cu2O+2H+���ʴ�Ϊ��FePO4+Li++e-��LiFePO4��2Cu+2H2O-2e-=Cu2O+2H+��
��2����Hf��Ka=
=6.4��10-4�������Ӻͷ�����Ũ������ȵģ�������Һ��H+Ũ��Ϊ
=8��10-3mol?L-1��������ĵ��볣����֪����������ǿ��HF���ε�ˮ����ɣ�Խ��Խˮ�⣻����F����ˮ��̶ȴ��ڴ�������ӵ�ˮ��̶ȣ�����NaF��Һ���������������ϴʴ�Ϊ��8��10-3������
����10mL0.1mol?L-1CH3COOH��Һ����εμ�0.1mol?L-1�İ�ˮ�������İ�ˮ10mLʱ���õ����Ǵ���淋�ˮ��Һ����ˮ�ĵ��볣���ʹ���ĵ��볣����ȣ�����笠����Ӻʹ�������ӵ�ˮ��̶���ȣ���Һ��ʾ���ԣ�����c��CH3COO-��=c��NH4+����c��H+��=c��OH-�����ʴ�Ϊ��c��CH3COO-��=c��NH4+����c��H+��=c��OH-����
�۸���NaH2PO4��Һ�����Զ�Na2HPO4��Һ�Լ��ԣ��õ�H2PO4-ˮ��̶�С�ڵ���̶ȣ������Ӷ�ˮ�ĵ������������ã�HPO4-ˮ��̶ȴ��ڵ���̶ȣ���ˮ�ĵ����ٽ����ã�����Na2HPO4��Һ��ˮ�ĵ���̶Ƚϴʴ�Ϊ�����ߴ�
| �ŵ� |
| ��� |
��2����Hf��Ka=
| c(H+)?c(F-) |
| c(HF) |
| 2 | Ka?c(HF) |
����10mL0.1mol?L-1CH3COOH��Һ����εμ�0.1mol?L-1�İ�ˮ�������İ�ˮ10mLʱ���õ����Ǵ���淋�ˮ��Һ����ˮ�ĵ��볣���ʹ���ĵ��볣����ȣ�����笠����Ӻʹ�������ӵ�ˮ��̶���ȣ���Һ��ʾ���ԣ�����c��CH3COO-��=c��NH4+����c��H+��=c��OH-�����ʴ�Ϊ��c��CH3COO-��=c��NH4+����c��H+��=c��OH-����
�۸���NaH2PO4��Һ�����Զ�Na2HPO4��Һ�Լ��ԣ��õ�H2PO4-ˮ��̶�С�ڵ���̶ȣ������Ӷ�ˮ�ĵ������������ã�HPO4-ˮ��̶ȴ��ڵ���̶ȣ���ˮ�ĵ����ٽ����ã�����Na2HPO4��Һ��ˮ�ĵ���̶Ƚϴʴ�Ϊ�����ߴ�
�����������ۺϿ���ѧ���绯ѧԭ���Լ��ε�ˮ��ԭ����������ʵĵ���ƽ��ȷ����֪ʶ�������ۺ�֪ʶ�Ŀ����⣬�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
��ҵ����ȡ�����Ҫ��Ӧ�У���2NaI+MnO2+3H2SO4�T2NaHSO4+MnSO4+2H2O+I2����2NaIO3+5NaHSO3�T2Na2SO4+3NaHSO4+H2O+I2�������й�˵����ȷ���ǣ�������
| A��I2�ڷ�Ӧ�����ǻ�ԭ����ڷ�Ӧ�������������� |
| B��NaHSO4��������Ӧ�о����������� |
| C��������Ӧ�����ɵ�����I2ʱת�Ƶĵ�������� |
| D��NaI��NaIO3��һ���������ܷ�Ӧ����I2 |
��֪�����������ݣ�7.2��10-4��4.6��10-4��4.9��10-10 �ֱ��������йص�������ĵ��볣��������֪���з�Ӧ���Է�����NaCN+HNO2=HCN+NaNO2 NaCN+HF=HCN+NaF NaNO2+HF=HNO2+NaF�ɴ˿��ж�������������ȷ���ǣ�������
| A��K��HF��=7.2��10-4 |
| B��K��HNO2��=4.9��10-10 |
| C������������Ӧ���ɵó����� |
| D��Ka��HCN����Ka��HNO2 �� |
�ö��Ե缫�������ͭ��Һһ��ʱ�������Һ�м���1mol Cu��OH��2��ǡ�ûָ���ԭ��Ũ�ȣ�����˵������ȷ���ǣ�������
| A������������Cu��H2 |
| B������������11.2L��O2 |
| C������������Һ��PHֵ���ϼ�С |
| D���������е���ת����Ŀ4NA |