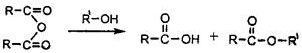题目内容
今有由铁的某种氧化物和铝粉组成的混合物X.为确定X中铁的氧化物的化学式 称取29.7gX隔绝空气高温下充分反应的混合物Y,Y与足量的氢氧化钠溶液反应收集到表准状况下气体3.36L,将反应液过滤、洗涤的固体Z将Z加入到120mL5mol?L-1 FeCl3溶液中,两者均恰好完全反应,则X中铁的氧化物为( )
| A、FeO |
| B、Fe3O4 |
| C、Fe2O3 |
| D、FeO2 |
考点:有关混合物反应的计算
专题:计算题
分析:反应后的固体能够与氢氧化钠溶液反应生成气体,该氢气只能为氢气,说明金属铝过量,铁的氧化物完全转化成铁单质;Z为铁,然后根据反应2Fe3++Fe=3Fe2+计算出生成铁的物质的量,根据氢气的量计算出反应后剩余铝的物质的量,然后根据质量守恒计算出反应生成氧化铝的质量,再计算出氧化铝的物质的量,从而得出氧化铁中氧元素的物质的量,从而得出该铁的氧化物的化学式.
解答:
解:标况下3.36L气体为Al与氢氧化钠溶液反应生成的氢气,其物质的量为:
=0.15mol,则反应消耗Al的物质的量为:0.15mol×
=0.1mol,
120mL5mol?L-1FeCl3溶液中含有含有氯化铁的物质的量为:n(FeCl3)=5mol/L×0.12L=0.6mol,根据反应2Fe3++Fe=3Fe2+可知,参加反应的铁的物质的量为:0.6mol×
=0.3mol,
Y能够与氢氧化钠溶液反应生成氢气,说明原混合物中铝过量,铁的氧化物完全反应,Y为金属铁、Al和氧化铝,其中铁的物质的量为0.3mol、铝为0.1mol,
根据质量守恒可知,Y中氧化铝的质量为:29.7g-56g/mol×0.3mol-27g/mol×0.1mol=10.2g,氧化铝的物质的量为:
=0.1mol,
氧化铝中氧元素来自氧化铁,所以氧化铁中氧元素的物质的量为:0.1mol×3=0.3mol,
该氧化铁中Fe与O元素的物质的量之比为:0.1mol:0.1mol=1:1,
所以该铁的氧化物为FeO,
故选A.
| 3.36L |
| 22.4L/mol |
| 2 |
| 3 |
120mL5mol?L-1FeCl3溶液中含有含有氯化铁的物质的量为:n(FeCl3)=5mol/L×0.12L=0.6mol,根据反应2Fe3++Fe=3Fe2+可知,参加反应的铁的物质的量为:0.6mol×
| 1 |
| 2 |
Y能够与氢氧化钠溶液反应生成氢气,说明原混合物中铝过量,铁的氧化物完全反应,Y为金属铁、Al和氧化铝,其中铁的物质的量为0.3mol、铝为0.1mol,
根据质量守恒可知,Y中氧化铝的质量为:29.7g-56g/mol×0.3mol-27g/mol×0.1mol=10.2g,氧化铝的物质的量为:
| 10.2g |
| 102g/mol |
氧化铝中氧元素来自氧化铁,所以氧化铁中氧元素的物质的量为:0.1mol×3=0.3mol,
该氧化铁中Fe与O元素的物质的量之比为:0.1mol:0.1mol=1:1,
所以该铁的氧化物为FeO,
故选A.
点评:本题考查了混合物反应的计算,题目难度中等,明确发生反应实质及反应原理为解答关键,注意质量守恒在化学计算或者的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
下列说法中,正确的是( )
| A、钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| D、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ |
14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,对上述反应下列各项判断正确的是( )
| A、反应中的氧化剂只有CuSO4 |
| B、7 mol CuSO4能氧化5mol-1价的硫 |
| C、被氧化的硫和被还原的硫个数之比是3:7 |
| D、FeS2既是氧化剂,又是还原剂 |
某不饱和烃的混合气体,其质量为相同状况下同体积H2的13.4倍,含有32g溴单质的溴水最多可吸收该混合气体2.24L(标准状况),则该混合烃是( )
| A、C2H4和C2H2 |
| B、C2H4和C3H4 |
| C、C3H4和C2H2 |
| D、C3H6和C3H4 |
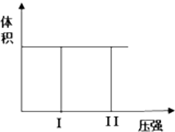 (Ⅰ) 在一个容积固定不变的密闭容器中进行反应:
(Ⅰ) 在一个容积固定不变的密闭容器中进行反应: