题目内容
18.下列物质按一定的分类方法属于同一类的是( )| A. | 酸性氧化物:CO2、SO2、SiO2、Na2O | B. | 盐:Na2CO3、KHCO3、Cu2(OH)2CO3 | ||
| C. | 非电解质:酒精、蔗糖、NH3、次氯酸 | D. | 混合物:液氯、盐酸、胆矾、氯水 |
分析 A.酸性氧化物是指和碱反应生成盐和水的氧化物,反应是复分解反应,生成的盐只有一种;
B.金属阳离子和酸根阴离子构成的化合物为盐;
C.水溶液中和熔融状态都不导电的化合物为非电解质;
D.不同物质组成的为混合物.
解答 解:A.CO2、SO2、SiO2、都是和碱反应生成盐和水氧化物属于酸性氧化物,Na2O是和酸反应生成盐和水的氧化物属于碱性氧化物,故A错误;
B.Na2CO3、KHCO3、Cu2(OH)2CO3 都是金属阳离子和酸根阴离子构成的化合物属于盐,故B正确;
C.酒精、蔗糖在水溶液中和熔融状态下都不导电属于非电解质,NH3本身不能电离出离子属于非电解质,次氯酸水溶液中存在电离平衡,水溶液导电,次氯酸属于电解质,故C错误;
D.液氯是一种物质组成的纯净物,盐酸是氯化氢气体的水溶液属于混合物,胆矾是硫酸铜晶体是一种物质组成属于纯净物,氯水是氯气的水溶液属于混合物,故D错误;
故选B.
点评 本题考查了物质分类、组成、名称、构成,注意了解概念实质和应用条件的应用,题目较简单.

练习册系列答案
相关题目
8.相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.
实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是ad
a.热量关系:a+b=92.4
b.三个容器内反应的平衡常数:③>①=②
c.平衡时氨气的体积分数:①=②>③
d.①N2的转化率+②NH3的转化率=100%
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 0 | 0 | 2 | 吸收热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
a.热量关系:a+b=92.4
b.三个容器内反应的平衡常数:③>①=②
c.平衡时氨气的体积分数:①=②>③
d.①N2的转化率+②NH3的转化率=100%
9.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法不正确的是( )
| A. | ClO2是还原产物 | |
| B. | H2C2O4在反应中被氧化 | |
| C. | 1molKClO3参加反应,转移电子物质的量为1mol | |
| D. | 生成5.6LCO2,转移的电子数目为0.25NA |
13.下列叙述正确的是( )
| A. | 提出原子结构模型的科学家按时间先后依次是:道尔顿、卢瑟福、汤姆生、玻尔 | |
| B. | 借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有哪些非金属元素 | |
| C. | 地球上大量的溴蕴藏在大海中,因此溴被称为“海洋元素” | |
| D. | 新制氯水应保存在无色试剂瓶中 |
3.下列状态的物质,既能导电又属于电解质的是( )
| A. | 盐酸 | B. | NH3 | C. | 熔融的K2O | D. | BaSO4晶体 |
10.下列说法正确的是( )
| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 | |
| C. | 用加热的方法可除去KNO3溶液中混有的FeCl3 | |
| D. | Na2CO3溶液加水稀释后,恢复至室温,pH和Kw均减小 |
8.最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”-全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的电子式为: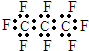 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 一个全氟丙烷分子中有10个共用电子对 |
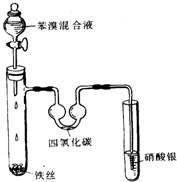 (1)苯分子中的碳碳之间的化学键是一种独特的键,因此其化学性质一般表现
(1)苯分子中的碳碳之间的化学键是一种独特的键,因此其化学性质一般表现