题目内容
3.下列状态的物质,既能导电又属于电解质的是( )| A. | 盐酸 | B. | NH3 | C. | 熔融的K2O | D. | BaSO4晶体 |
分析 电解质是水溶液中或熔融状态下都导电的化合物,物质导电的条件:存在自由电子或者自由移动的离子,据此解答.
解答 解:A.盐酸是氯化氢气体的水溶液,溶液导电是混合物,不是电解质,故A不选;
B.NH3本身不能电离出自由移动的离子,属于非电解质,故B不选;
C.熔融的K2O,本身能够电离产生自由移动离子而导电,属于电解质,故C选;
D.硫酸钡晶体不能导电,熔融状态下完全电离属于强电解质,故D错误;
故选C.
点评 本题考查了电解质的判断,熟悉电解质的概念是解题关键,注意电解质一定是化合物,单质、混合物既不是电解质,也不是非电解质,题目较简单.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
14.氰化物有剧毒,工业废水中氰化物(CN-)的最高允许排放浓度为0.5mg/L;对废水中CN-(N为-3价)的处理方法是:在碱性条件下,用Cl2将废水中的CN-转化成N2和CO2等,使废水得到净化.发生的反应为:2CN-+8OH-+5Cl2═2CO2↑+N2↑+10Cl-+4H2O.下列有关说法正确的是( )
| A. | 上述反应中氧化产物只有N2 | |
| B. | 当有0.4molCO2生成时,反应中转移的电子的总数目约为1.204×1024 | |
| C. | 若上述反应生成0.4molCO2,则溶液中阴离子增加的物质的量为2mol | |
| D. | 现取1L含CN-1.02mg/L的废水,至少需用4.0×10-5molCl2处理后才符合排放标准 |
18.下列物质按一定的分类方法属于同一类的是( )
| A. | 酸性氧化物:CO2、SO2、SiO2、Na2O | B. | 盐:Na2CO3、KHCO3、Cu2(OH)2CO3 | ||
| C. | 非电解质:酒精、蔗糖、NH3、次氯酸 | D. | 混合物:液氯、盐酸、胆矾、氯水 |
8.下列说法正确的是( )
| A. | 钠保存在煤油里的原因之一是它极易与氧气反应 | |
| B. | 铝在空气中很容易燃烧 | |
| C. | 镁表面的氧化膜疏松,不能保护内层金属 | |
| D. | 铁锈的主要成分是Fe3O4 |
15.下列说法正确的是( )
| A. | CaCl2是中性干燥剂可以干燥NH3、SO2 | |
| B. | 检查病人胃病所用的钡餐,既可以用BaSO4,也可以用BaCO3 | |
| C. | 氮氧化物的大量排放是造成光化学烟雾的主要原因 | |
| D. | 雨水样品放置一段时间后,酸性增强的原因是因为溶解了空气中的CO2 |
12.下列各组物质的燃烧热相等的是( )
| A. | 碳和二氧化碳 | B. | 1mol 碳和3mol 碳 | ||
| C. | 3mol C2H2和1mol C6H6 | D. | 淀粉和纤维素 |
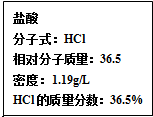 化学与人们生活质量的提高以及社会发展有着密切的关系.
化学与人们生活质量的提高以及社会发展有着密切的关系.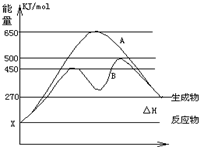 反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示.试回答:
反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示.试回答: