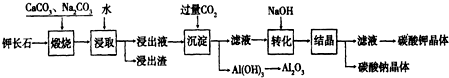
题目内容
3.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.回答下列问题:(1)基态砷原子的电子排布式为1s22s22p63s23p63d104s24p3.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间化学键类型为配位键,与CN-互为等电子体的化合物分子式为CO.
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染.光化学烟雾中含有NOx,、O3、CH2═CHCHO、HCOOH、
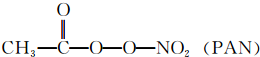 等二次污染物.
等二次污染物.①N2O结构式可表示为N═N═O,N2O中中心氮原子的杂化轨道类型为sp,l molPAN中含σ键数目为10NA.
②测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr.Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个.晶胞中含K r原子为n个,则$\frac{m}{n}$=3(填数字).已知Kr晶体的密度为ρg/cm3,摩尔质量为Mg/mol.阿伏加德罗常数用NA表示,列式表示Kr晶胞参数α=$\root{3}{\frac{4M}{ρ{N}_{A}}}$×10-7nm.
分析 (1)As原子核外电子数为33,根据能量最低原理书写核外电子排布式;
(2)Fe3+可以空轨道,CN-含有孤对电子,二者形成配位键;与CN-互为等电子体的化合物含有2个原子、价电子总数为10;
(3)①N2O结构式可表示为N═N═O,N2O中中心N原子形成2个σ键、没有孤对电子,杂化轨道数目为2;
单键为σ键,双键含有1个σ键、1个π键,PAN分子中σ键数目为10;
②Kr晶体为面心立方晶体,以顶点Kr原子研究,与之相邻的Kr原子处于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,利用均摊法计算晶胞中Kr原子数目、晶胞中Kr原子配位数,结合晶胞中含有Kr原子数目,表示出晶胞质量,再结合m=ρV计算晶胞棱长.
解答 解:(1)As原子核外电子数为33,根据能量最低原理,核外电子排布式为:1s22s22p63s23p63d104s24p3,
故答案为:1s22s22p63s23p63d104s24p3;
(2)Fe3+含有空轨道,CN-含有孤对电子,二者之间形成配位键;原子数目相等、价电子数目相等的微粒互为等电子体,与CN-互为等电子体的化合物分子式为CO,
故答案为:配位;CO;
(3)①N2O结构式可表示为N=N=O,N2O中中心氮原子形成2个σ键、没有孤对电子,杂化轨道数目为2,N原子采取sp杂化;单键为σ键,双键含有1个σ键、1个π键,PAN分子中σ键数目为10,则l mol PAN中含σ键数目为10NA,
故答案为:sp;10NA;
②Kr晶体为面心立方晶体,以顶点Kr原子研究,与之相邻的Kr原子处于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,晶体中与每个Kr原子相紧邻的Kr原子数为$\frac{3×8}{2}$=12,晶胞中Kr原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则$\frac{m}{n}$=3;
晶胞质量为4×$\frac{M}{{N}_{A}}$g,晶体的密度为ρg/cm3,则ρg/cm3×(a×10-7 cm)3=4×$\frac{M}{{N}_{A}}$g,解得a=$\root{3}{\frac{4M}{ρ{N}_{A}}}$×10-7,
故答案为:3;$\root{3}{\frac{4M}{ρ{N}_{A}}}$×10-7.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、配合物、等电子体、杂化方式、化学键、晶胞计算等,是都物质结构主干知识考查,(3)中计算需要学生具备一定的空间想象,理解掌握用均摊法进行晶胞有关计算.

| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将铝丝放入浓硫酸中 | 无明显现象 | 铝丝发生了钝化 |
| B | 将SO2通入过量的Na2CO3溶液中,将产生的气体再通入Na2SiO3溶液中 | 有白色沉淀生成 | 证明酸性:H2SO3>H2CO3>H2SiO3 |
| C | 向含有Fe3+的溶液中滴加KSCN溶液 | 溶液变红色 | 有Fe(SCN)3生成 |
| D | 向KOH溶液中滴加足量的MgSO4溶液,然后再滴加足量的FeCl3溶液 | 先产生白色沉淀,然后沉淀变红褐色 | Ksp[Fe(OH)3]>Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
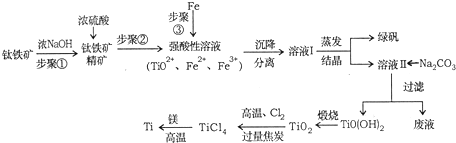
已知:①2H2SO4(浓)+FeTiO3=TiOSO4+FeSO4 +2H2O
②TiO2+易水解,只能存在于强酸性溶液中.
(1)步骤①中发生反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O,SiO2+2OH-=SiO32-+H2O.
(2)25℃时,难溶电解质形成沉淀与pH关系如下表
| PH | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | TiO(OH)2 |
| 开始沉淀 | 1.1 | 4.5 | 7 | 1 |
| 完全沉淀 | 2.8 | 6.4 | 9.2 | 2.7 |
a.步骤①加入铁屑原因是将Fe3+转化为Fe2+,防止Fe3+与TiO2+同时生成沉淀.
b.向溶液Ⅱ中加入Na2CO3粉末的作用是调节PH,生成TiO(OH)2溶液.溶液Ⅱ中大量含有的阳离子有TiO2+、Fe2+、H+.
(3)TiCl4→Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti.
①写出由TiO2制取TiCl4的化学方程式TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.
②依据下表信息,需加热的温度略高于1412℃即可.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/ | 136.4 | 1090 | 1412 | 3287 |
| A. | C57H104O6 | B. | C57H108O6 | C. | C57H106O6 | D. | C57H102O6 |
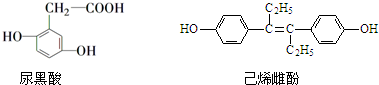
| A. | 尿黑酸分子中所有碳原子一定都在同一平面内 | |
| B. | 己烯雌酚可发生加成、取代、氧化、加聚、酯化反应 | |
| C. | 尿黑酸和己烯雌酚都属于芳香族化合物 | |
| D. | 各1mol的尿黑酸和己烯雌酚分别最多能消耗3mol 和6mol Br2 |
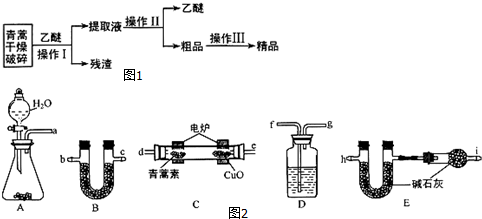
请回答下列问题:
(1)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作Ⅰ用到的玻璃仪器是漏斗、玻璃棒、烧杯,操作Ⅱ的名称是蒸馏.
(3)用如图2的实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
①仪器各接口的连接顺序从左到右依次为afgdebchi(每个装置限用一次).
②装置C中CuO的作用是使青蒿素充分氧化生成CO2和H2O.
③装置D中的试剂为浓硫酸.
④已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是C(填字母代号).
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.
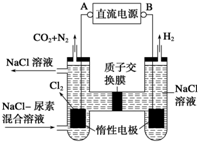
| A. | A 极为电源的负极 | |
| B. | 阳极室中发生的反应只有CO(NH2)2-6e-+6OH -=N2↑+CO2↑+5H2O | |
| C. | 阴极室溶液的 PH 电解前后保持不变 | |
| D. | 除去 3.6 克尿素时阴极一定生成 H26.72L |
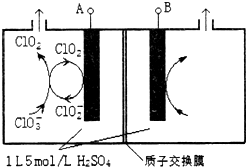 二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”.工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2.
二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”.工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2.