题目内容
3.下列实验操作、实验现象和解释或结论不正确的是( )| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将铝丝放入浓硫酸中 | 无明显现象 | 铝丝发生了钝化 |
| B | 将SO2通入过量的Na2CO3溶液中,将产生的气体再通入Na2SiO3溶液中 | 有白色沉淀生成 | 证明酸性:H2SO3>H2CO3>H2SiO3 |
| C | 向含有Fe3+的溶液中滴加KSCN溶液 | 溶液变红色 | 有Fe(SCN)3生成 |
| D | 向KOH溶液中滴加足量的MgSO4溶液,然后再滴加足量的FeCl3溶液 | 先产生白色沉淀,然后沉淀变红褐色 | Ksp[Fe(OH)3]>Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
分析 A.常温下,铝与浓硫酸发生钝化反应;
B.二氧化硫与碳酸钠溶液反应生成二氧化碳,二氧化碳都能与硅酸钠溶液反应生成硅酸沉淀;
C.发生Fe3++3SCN-?Fe(SCN)3;
D.从难溶电解质的平衡移动的角度判断.
解答 解:A.常温下,铝与浓硫酸发生钝化反应,没有明显的反应现象,故A正确;
B.二氧化硫与碳酸钠溶液反应生成二氧化碳,二氧化碳都能与硅酸钠溶液反应生成硅酸沉淀,所以能证明H2SO3>H2CO3>H2SiO3,故B正确;
C.Fe3+与KSCN溶液反应生成红色溶液,发生反应Fe3++3SCN-=Fe(SCN)3,故C正确;
D.向KOH溶液中滴加足量的MgSO4溶液,然后再滴加足量的FeCl3溶液,先产生白色沉淀,然后沉淀变红褐色,可说明氢氧化镁转化为氢氧化铁,氢氧化铁更难溶,则Ksp[Fe(OH)3]<Ksp[Mg(OH)2],故D错误.
故选D.
点评 本题考查化学实验方案的评价,涉及物质性质比较、检验、难溶电解质的平衡移动等知识,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型和高频考点,注意把握实验的严密性和合理性,难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
13.25℃时,某溶液中可能含有以下几种离子:Na+、H+、Fe3+、HCO${\;}_{3}^{-}$、OH-、I-.已知溶液中由水电离出的c(H+)=10-13mol•L-1,向该溶液中通入一定量的Cl2后,溶液由无色变为黄色,下列有关该溶液的说法中正确的是( )
| A. | 该溶液的pH一定等于1 | |
| B. | 阴离子肯定有I-,不能确定有无HCO${\;}_{3}^{-}$ | |
| C. | 阳离子肯定没有Fe3+,一定有Na+ | |
| D. | 该溶液含有的溶质成分可能为HI;或HI和NaI;或NaI和NaOH |
18.下表为各物质中所含有的少量杂质以及除去这些杂质应选用的试剂或操作方法,正确的一组为( )
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| A | C2H5Br | C2H5OH | 用水洗涤、分液 |
| B | FeCl3 | CaCO3 | 溶解、过滤、蒸发结晶 |
| C | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
| D | CO2 | SO2 | 通过盛有品红溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
8.下列物质中,其主要成分不属于烃的是( )
| A. | 汽油 | B. | 甘油 | C. | 煤油 | D. | 柴油 |
15.下列有关实验操作的叙述错误的是( )
| A. | 过滤操作中,漏斗的尖端应接触烧杯内壁 | |
| B. | 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 | |
| C. | 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 | |
| D. | 向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁 |
2.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
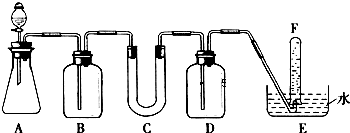
(1)A是利用盐酸和石灰石制取CO2的装置,A中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
在此反应中,过氧化钠的作用是③(填序号) ①氧化剂;②还原剂;③既是氧化剂又是还原剂;④既不是氧化剂,又不是还原剂.
(4)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂.

(1)A是利用盐酸和石灰石制取CO2的装置,A中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | ||
| D |
在此反应中,过氧化钠的作用是③(填序号) ①氧化剂;②还原剂;③既是氧化剂又是还原剂;④既不是氧化剂,又不是还原剂.
(4)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂.

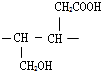 ;
;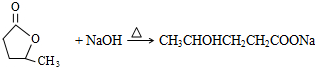 ;
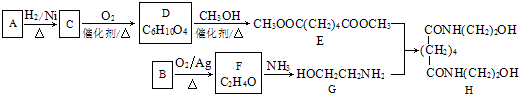
;
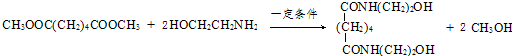 .
.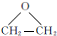 ,能发生银镜反应的F的同分异构体是CH3CHO.
,能发生银镜反应的F的同分异构体是CH3CHO.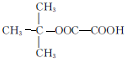 (写结构简式).
(写结构简式).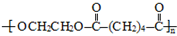 的合成路线.
的合成路线.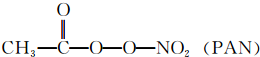 等二次污染物.
等二次污染物.