题目内容
8.尿黑酸和己烯雌酚的结构简式如下:下列说法正确的是( )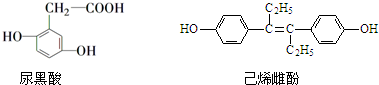
| A. | 尿黑酸分子中所有碳原子一定都在同一平面内 | |
| B. | 己烯雌酚可发生加成、取代、氧化、加聚、酯化反应 | |
| C. | 尿黑酸和己烯雌酚都属于芳香族化合物 | |
| D. | 各1mol的尿黑酸和己烯雌酚分别最多能消耗3mol 和6mol Br2 |
分析 A、羧基上的碳与苯环上的碳可能在同一平面上;
B、己烯雌酚分子中含有双键和苯环可发生加成、氧化、加聚;含酚羟基发生取代和酯化反应;
C、含苯环的化合物是芳香族化合物;
D、1mol的尿黑酸和3molBr2发生取代反应,1mol的己烯雌酚和1mol Br2加成4molBr2发生取代反应.
解答 解:A、羧基上的碳与苯环上的碳可能在同一平面上,所以不一定在同一平面上,故A错误;
B、己烯雌酚分子中含有双键和苯环可发生加成、氧化、加聚;含酚羟基发生取代和酯化反应,所以己烯雌酚可发生加成、取代、氧化、加聚、酯化反应,故B正确;
C、两种有机物中都是含苯环的化合物是芳香族化合物,故C正确;
D、1mol的尿黑酸和3molBr2发生取代反应,1mol的己烯雌酚和1mol Br2加成4molBr2发生取代反应,所以分别最多能消耗3mol 和5mol Br2,故Q错误;
故选BC.
点评 本题考查有机物的结构决定性质,熟记官能团所具有的性质是解题的关键所在,比较容易.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
8.下列物质中,其主要成分不属于烃的是( )
| A. | 汽油 | B. | 甘油 | C. | 煤油 | D. | 柴油 |
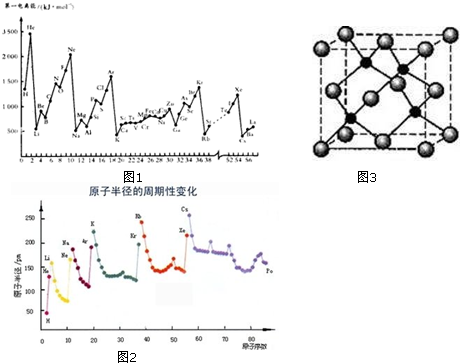
17.短周期元素 A、B、C、D、E 的原子序数依次增大;A 的一种核素在考古时常用来鉴定一些文物的年代,B的氢化物的水溶液呈碱性;C、D为金属元素,且D原子最外层电子数等于其 K 层电子数;若往 E 单质的水溶液中滴加少量紫色石蕊试液,可观察到先变红后褪色.下列说法中,正确的是( )
| A. | B的最高价氧化物对应的水化物的酸性比E强 | |
| B. | 某物质焰色反应呈黄色,该物质一定是含C的盐 | |
| C. | 向D单质与沸水反应后的溶液中滴加酚酞,溶液变红 | |
| D. | B的氢化物的沸点一定高于A的氢化物 |
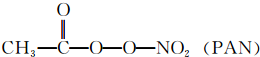 等二次污染物.
等二次污染物.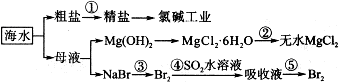
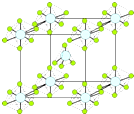 磷元素在生产和生活中有广泛的应用.
磷元素在生产和生活中有广泛的应用.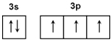 .
.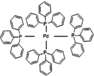 ):P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为sp3;判断该物质在水中溶解度并加以解释不易溶于水.水为极性分子,四(三苯基膦)钯分子为非极性分子,分子极性不相似,故不相溶.该物质可用于如图所示物质A(
):P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为sp3;判断该物质在水中溶解度并加以解释不易溶于水.水为极性分子,四(三苯基膦)钯分子为非极性分子,分子极性不相似,故不相溶.该物质可用于如图所示物质A(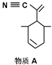 )的合成:物质A中碳原子杂化轨道类型为sp、sp2、sp3;一个A分子中手性碳原子数目为3.
)的合成:物质A中碳原子杂化轨道类型为sp、sp2、sp3;一个A分子中手性碳原子数目为3. )都是生活中常见的有机物,请按要求完成下列问题;
)都是生活中常见的有机物,请按要求完成下列问题;