题目内容
下列实验方案设计合理且能达到相应实验预期目的是( )
A、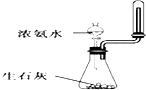 制取少量氨气 |
B、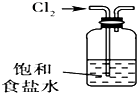 除去氯气中的HCl杂质 |
C、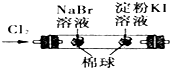 证明氧化性Cl2>Br2>I2 |
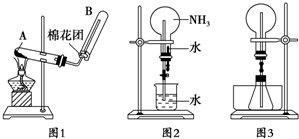
D、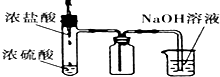 制取HCl且除去多余的气体 |
考点:化学实验方案的评价
专题:
分析:A.收集气体的试管不能使用塞子;
B.HCl极易溶于水,导管长进短出;
C.氯气与NaBr、NaI均可发生氧化还原反应;
D.尾气处理时可发生倒吸.
B.HCl极易溶于水,导管长进短出;
C.氯气与NaBr、NaI均可发生氧化还原反应;
D.尾气处理时可发生倒吸.
解答:
解:A.收集试管带塞子不能收集气体,气体过多可能导致试管炸裂,故A错误;
B.HCl极易溶于水,导管长进短出,且食盐水抑制氯气的溶解,除杂装置合理,故B正确;
C.氯气能与碘化钾反应,应将溴单质中的氯气除掉,不能比较Br2>I2,故C错误;
D.导管不能插入液面下,以免发生倒吸,故D错误;
故选B.
B.HCl极易溶于水,导管长进短出,且食盐水抑制氯气的溶解,除杂装置合理,故B正确;
C.氯气能与碘化钾反应,应将溴单质中的氯气除掉,不能比较Br2>I2,故C错误;
D.导管不能插入液面下,以免发生倒吸,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及洗气、气体的制取及收集、氧化性的比较、气体制取的实验,侧重实验细节的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
久置在空气中不会变质的物质是( )
| A、硫酸亚铁 | B、硫酸钠 |
| C、过氧化钠 | D、漂白粉 |
现有1.0mol/L的NaOH溶液0.1L,若通入标准状况下体积为2.24L 的SO2气体,使其充分反应后,则所得溶液中各粒子浓度大小关系正确的是( )
| A、c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c( OH-) |
| B、c(Na+)=c(H2SO3)+c(HSO3-)+c( H+) |
| C、c(SO32-)+c( OH-)=c(H+)+c(H2SO3) |
| D、c(Na+)>c(HSO3-)>c( OH-)>c(H2SO3)>c(SO32-)>c(H+) |
下列各组中的离子能在溶液中大量共存,向溶液中加入NaOH溶液时产生沉淀,且加入盐酸时放出气体的离子组是( )
| A、OH-、Ba2+、NO3-、K+ |
| B、Fe2+、Ca2+、Br-、NO3- |
| C、Na+、SO42-、Cu2+、Cl- |
| D、CO32-、Cl-、Na+、Ba2+ |
粗食盐的杂质主要是MgCl2.为了除去杂质,工业上常把粗盐粉碎后用饱和食盐水浸洗,再过滤出食盐.对此,下面的评论正确的是( )
| A、浸洗前后,被浸洗的食盐中MgCl2的含量基本不变 |
| B、用来浸洗的饱和食盐水在浸洗前后没有变化 |
| C、浸洗用过的饱和食盐水可以无限次地使用下去 |
| D、粉碎颗粒的大小影响浸洗后盐中MgCl2的含量 |
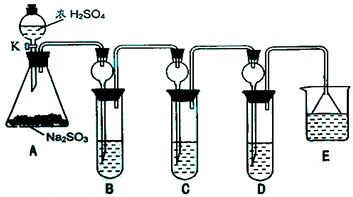 某研究小组欲探究SO2的化学性质,设计了如右图所示实验方案.
某研究小组欲探究SO2的化学性质,设计了如右图所示实验方案.