题目内容
20.下列说法错误的是( )| A. | NaClO溶液中:c(Na+)=c(ClO-)+c(OH-)+c(HClO) | |
| B. | 常温下,pH=a的NH4Cl溶液中由水电离产生的c(OH-)=10-amol•L-1 | |
| C. | 向0.1 mol•L-1的Na2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| D. | Na2S稀溶液中:c(OH-)=c(H+)+2c(H2S)+c(HS-) |
分析 A.根据物料守恒分析;
B.NH4Cl溶液中氢离子全部由水电离;
C.Na2SO3溶液中加入少量NaOH固体,氢氧化钠抑制亚硫酸根离子的水解;
D.根据溶液的质子守恒分析.
解答 解:A.NaClO溶液中,钠元素的总浓度等于氯元素的总浓度,则溶液中物料守恒为:c(Na+)=c(ClO-)+c(HClO),故A错误;
B.NH4Cl溶液中氢离子全部由水电离,则常温下,pH=a的NH4Cl溶液中由水电离产生的c(OH-)=10-amol•L-1,故B正确;
C.Na2SO3溶液中加入少量NaOH固体,氢氧化钠抑制亚硫酸根离子的水解,溶液中c(SO32-)增大,加入NaOH溶液,c(Na+)也增大,故C正确;
D.Na2S稀溶液中,存在质子守恒,即:c(OH-)=c(H+)+2c(H2S)+c(HS-),故D正确.
故选A.
点评 本题考查了盐的水解、以及影响水解平衡的因素,题目难度不大,注意把握溶液中的物料守恒和质子守恒等守恒关系的应用,侧重于考查学生的综合应用能力.

练习册系列答案
相关题目
10.下列酸溶液的pH相同时,其物质的量浓度最小的是( )
| A. | H2S | B. | H2SO4 | C. | HClO | D. | HNO3 |
11.下列说法正确的是( )
| A. | 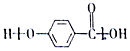 的结构中含有酯基 的结构中含有酯基 | |
| B. | 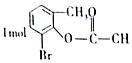 一定条件下与足量NaOH溶液反应,最多消耗3molNaOH 一定条件下与足量NaOH溶液反应,最多消耗3molNaOH | |
| C. | 按系统命名法,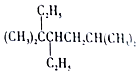 的名称为3,3,6-三甲基-4-乙基庚烷 的名称为3,3,6-三甲基-4-乙基庚烷 | |
| D. | 油脂和蛋白质都是能发生水解反应的高分子化合物 |
8.化学与材料、生活和环境密切相关,下列有关分类中正确的是( )
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| C. | 蛋白质、淀粉、纤维素都属于有机高分子化合物 | |
| D. | 天然纤维和合成纤维的主要成分是纤维素 |
9.下列物质不含官能团的是①(CH3)3C-CH3 ②CH2=CH2 ③CH≡CH ④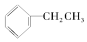 ⑤CH3COOCH3 ⑥
⑤CH3COOCH3 ⑥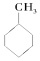
 ⑤CH3COOCH3 ⑥
⑤CH3COOCH3 ⑥
| A. | ②③⑤ | B. | ①⑤⑥ | C. | ①④⑥ | D. | ①④⑤ |
10.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12.某溶液中含有Cl-,Br-,CrO4-,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
| A. | I-、Br-、CrO4- | B. | Br-、Cl-、CrO4- | C. | CrO4-、Br-、I- | D. | Br-、CrO4-、Cl- |