题目内容
4.如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
| A. | 该硫酸试剂可以做干燥剂,干燥任何气体 | |
| B. | 稀释该硫酸时,应将蒸馏水沿玻璃棒缓慢注入其中 | |
| C. | 常温下,2.7g Al与足量的稀硫酸反应得到H23.36L | |
| D. | 配制200mL 4.6mol•L-1的稀硫酸需取该硫酸50.0mL |
分析 A.硫酸为酸性物质,不能干燥碱性气体;
B.稀释浓硫酸时,应该将浓硫酸加入水中;
C.没有指出在标准状况下,不能用标准状况下的气体摩尔体积计算;
D.先根据c=$\frac{1000ρω}{M}$计算出该浓硫酸的浓度,配制过程中溶质的物质的量不变,据此计算出需要浓硫酸的体积.
解答 解:A.浓硫酸能够干燥酸性气体,不能干燥碱性的气体,如氨气,故A错误;
B.稀释该硫酸时,应将浓硫酸沿玻璃棒缓慢加入水中,顺序不能颠倒,故B错误;
C.不是标准状况下,不能使用标准状况下的气体摩尔体积计算,故C错误;
D.该浓硫酸的浓度为:$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,配制过程中硫酸的物质的量不变,则配制200mL 4.6mol•L-1的稀硫酸需取该硫酸体积为:$\frac{4.6mol/L×0.2L}{18.4mol/L}$=0.05L=50.0mL,故D正确;
故选D.
点评 本题考查了物质的量浓度的计算,题目难度不大,涉及物质的量浓度的计算、干燥剂的选用、标准状况下气体摩尔体积的使用条件等知识,C为易错点,注意明确标准状况下气体摩尔体积的使用条件,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
2.糖类、油脂和蛋白质是人体所需的三大基本营养物质,下列说法中错误的是( )
| A. | 糖类、油脂和蛋白质都属于高分子化合物 | |
| B. | 淀粉、油脂和蛋白质都能发生水解反应 | |
| C. | 油脂有油和脂肪之分,但都属于酯 | |
| D. | 蛋白质既能与酸反应又能与碱反应 |
19.下列离子方程式书写正确的是( )
| A. | 用Cu片作阳极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+H2↑+2OH- | |
| B. | 用两个铜片作电极电解AgNO3溶液:4Ag++2H2O$\frac{\underline{\;电解\;}}{\;}$Ag+O2+4H+ | |
| C. | 用石墨作电极电解AlCl3溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 用石墨作电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ |
6.下列说法正确的是( )
| A. | 小苏打的主要成分是碳酸钠 | |
| B. | NaHCO3的热稳定性小于Na2CO3 | |
| C. | KCl和Na2CO3的固体混合物,加水溶解时有沉淀生成,且沉淀溶于稀盐酸 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀,其离子方程式可以表示为:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+H2O |
16.下列说法正确的是( )
| A. | 离子化合物中一定不含共价键 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 金属元素和非金属元素之间形成的化学键一定是离子键 |
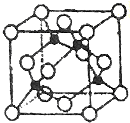 周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均己充满电子.请回答下列问题:
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均己充满电子.请回答下列问题: 全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟.如图是钒电池基本工作原理示意图:
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟.如图是钒电池基本工作原理示意图: