题目内容
5.2015年10月,中国女药学家屠呦呦由于在创制新型抗疟药--青蒿素和双氢青蒿素中的巨大贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.化学药物在抗击疾病、保护人体健康中发挥了重要作用.(1)1928年英国细菌学家弗莱明首先发现了世界上第一种抗生素--青霉素.
①青霉素是最重要的抗生素,目前广泛使用的羟氨苄青霉素,又名B(填字母);
A.阿司匹林 B.阿莫西林 C.阿奇霉素
②为了防止“过敏反应”的发生,在使用青霉素前需要B(填字母);
A.静脉滴注NaHCO3溶液 B.进行皮肤敏感试验 C.服用镇静催眠药
③青霉素属于R处方药(填“R处方药”或“OTC非处方药”).
(2)抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质.
①这些抗酸药物具有抗酸作用的原因是抗酸药物有效成分能中和胃里过多的盐酸.
②某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉.写出该抗酸药发挥功效时的化学方程式Al(OH)3+3H+═Al3++3H2O.(写出其中一个即可)
③淀粉在抗酸药中作为填充剂和黏合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)C6H12O6
(3)许多药物可以通过对天然药物的化学结构进行修饰得到.下列属于化学结构修饰得到的药物是AC.

分析 (1)①羟氨苄青霉素又名阿莫西林;
②青霉素在使用前要作皮试;
③处方药是必须凭执业医师或执助理医师才可调配、购买和使用的药品;
(2)根据抗酸药物有效成分能中和胃里过多的盐酸分析;淀粉在人体内在酶的作用水解最终转化成葡萄糖;
(3)在合成阿司匹林和阿莫西林时对结构进行了修饰.
解答 解:(1)①羟氨苄青霉素又名阿莫西林,是常用的抗生素,故答案为:B;
②在使用青霉素前需要进行皮肤敏感试验,即做皮试,故答案为:B;
③青霉素属于R处方药,故答案为:R处方药;
(2)碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁都能中和胃里过多的盐酸;氢氧化铝和盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH)3+3H+═Al3++3H2O;淀粉的化学式可用(C6H10O5)n表示,淀粉在人体内在酶的作用水解最终转化成葡萄糖,其化学式为:C6H12O6,
故答案为:抗酸药物有效成分能中和胃里过多的盐酸;Al(OH)3+3H+═Al3++3H2O;C6H12O6;
(3)在合成阿司匹林和阿莫西林时对结构进行了修饰,故选AC.
点评 本题考查药物的主要成分和疗效、有机物的结构与性质,注意习题中的信息分析物质的性质,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
1.下列离子方程式中,不正确的是( )
| A. | 高锰酸钾酸性溶液与草酸钾溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| B. | KI的酸性溶液长期置于空气中::4I-+4H++O2═2I2+2H2O | |
| C. | 硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O | |
| D. | 用食醋除去水垢:CO32-+2CH3COOH═H2O+CO2↑+2CH3COO- |
2.以下对电子转移的方向和数目的表示正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
13.随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.
(l)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g) $\stackrel{RU}{?}$CH4(g)+2H2O(g)
已知CO2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列各物理量的变化.(选填“增大”、“减小”或“不变”)
v正增大,v逆增大,平衡常数K减小,转化率α减小.
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
a、b、c、d与m、n、x、y之间的关系式为$\frac{c{d}^{2}}{a{b}^{4}}$=$\frac{x{y}^{2}}{m{n}^{4}}$.
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3-?H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象.当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变
(4)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2 4KO2+4CO2+2H2O→4KHCO3+3O2
若9molCO2在密封舱内和KO2反应后生成9molO2,则反应前密封舱内H20的量应该是3mol.
(l)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g) $\stackrel{RU}{?}$CH4(g)+2H2O(g)
已知CO2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列各物理量的变化.(选填“增大”、“减小”或“不变”)
v正增大,v逆增大,平衡常数K减小,转化率α减小.
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3-?H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象.当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变
(4)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2 4KO2+4CO2+2H2O→4KHCO3+3O2
若9molCO2在密封舱内和KO2反应后生成9molO2,则反应前密封舱内H20的量应该是3mol.
20.采自地质深层的矿泉水常溶有岩石所含放射性物质在衰变过程中释放的氡,下列关于该类矿泉水说法正确的是( )
| A. | 该矿泉水越鲜越好 | |
| B. | 该矿泉水宜存放一段时间再用 | |
| C. | 鲜用和存放一段使用对人体危害是一样的 | |
| D. | 越深层开采矿泉水,污染程度越小 |
10. 中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )
中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )
 中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )
中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )| A. | 分子式为C14H18O6 | |
| B. | 环上氢原子的一氯取代物5种 | |
| C. | 1mol该有机物与足量的金属钠反应产生4mol H2 | |
| D. | 分子间能发生酯化反应 |
17.下列关于物质的浓度的说法正确的是( )
| A. | 将5.85 g NaCl固体溶于1 L水中可配成0.1mol/L的NaCl 溶液 | |
| B. | 500 ml 0.5mol/L 的NaOH溶液含NaOH分子0.25 mol | |
| C. | 把200mL 3mol/L的BaCl2溶液跟100mL 3mol/L的KCl溶液混合后,溶液中的c(Cl-)仍然是3mol/L(忽略混合后体积变化) | |
| D. | 把100g 20%的NaCl溶液跟100g H2O混合后,NaCl溶液的质量分数是10% |
14.某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:下列说法中正确的是( )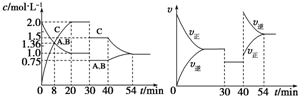

| A. | 30~40 min 间该反应使用了催化剂 | |
| B. | 反应方程式中的x=1,正反应为吸热反应 | |
| C. | 30 min 时降低温度,40 min 时升高温度 | |
| D. | 30 min时减小压强,40 min时升高温度 |