题目内容
14.某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:下列说法中正确的是( )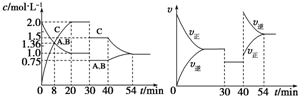
| A. | 30~40 min 间该反应使用了催化剂 | |
| B. | 反应方程式中的x=1,正反应为吸热反应 | |
| C. | 30 min 时降低温度,40 min 时升高温度 | |
| D. | 30 min时减小压强,40 min时升高温度 |
分析 由图象可知,30min-40min之间,反应速率降低了,平衡不移动,反应物与生成物的浓度瞬时降低,催化剂不能改变浓度,故不能是温度变化,而是降低了压强;
由开始到达到平衡,A、B的浓度减少的量相同,由此可知x=1.则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应,以此解答该题.
解答 解:A.由图象可知,30~40 min只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强,故A错误;
B.由开始到达到平衡,A、B的浓度减少的量相同,由此可知x=1,反应前后气体体积不变,则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡逆向移动,应是升高温度,则正反应为放热反应,故B错误;
C.降低温度,平衡发生移动,则正逆反应速率不相等,故C错误;
D.由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,故D正确.
故选D.
点评 本题考查化学平衡图象,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意图象中反应速率的变化及平衡移动,明确温度、浓度、压强对反应速率及平衡的影响即可解答,题目难度中等.

练习册系列答案
相关题目
10.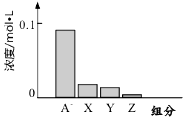 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中都分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中都分微粒组分及浓度如图所示,下列说法正确的是( )
 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中都分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中都分微粒组分及浓度如图所示,下列说法正确的是( )| A. | HA为强酸 | B. | 该混合液pH=7 | ||
| C. | 图中X表示HA,Y表示OH-,Z表示H+ | D. | 该混合溶液中:c(A-)+c(Y)=c(Na+) |
9.下列各项表述中正确的是( )
| A. | 氢氧燃料电池就是将氢气在氧气中燃烧,从而获得电流 | |
| B. | 46g的乙醇和28g的乙烯完全燃烧时消耗的O2均为为67.2L(标准状况) | |
| C. | 在氮原子中,质子数为7而中子数一定也为7 | |
| D. | Cl-的结构示意图为 |
19.已知,氧气与不同聚集状态的硫单质反应的热化学方程式如下:
①S(s)+O2(g)=SO2(g)△H=a kJ/mol;
②S(g)+O2(g)=SO2(g)△H=b kJ/mol;
对于a和b的关系,下列说法正确的是( )
①S(s)+O2(g)=SO2(g)△H=a kJ/mol;
②S(g)+O2(g)=SO2(g)△H=b kJ/mol;
对于a和b的关系,下列说法正确的是( )
| A. | a>0,b>0 | B. | a<0,b<0 | C. | a>b | D. | a<b |
3.形成合金的叙述错误的是( )
| A. | 形成合金后,其熔点要提高 | B. | 合金是混合物 | ||
| C. | 合金具有固定的熔点 | D. | 铁与非金属氯,氧等很难形成合金 |
