题目内容
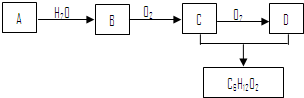
8.表为元素周期表的一部分:| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(1)画出元素②的离子结构示意图
 .
.(2)②、③、⑤的离子半径由大到小的顺序为S2->O2->Na+.
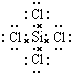
(3)元素④和⑥形成的化合物的电子式:
 .
.
分析 根据元素周期表结构可知,①为H元素、②为O元素、③为Na元素、④为Si元素、⑤为S元素、⑥为Cl元素,
(1)②为O元素,氧离子的核电荷数为8,核外电子总数为10,最外层达到8电子稳定结构,据此画出离子结构示意图;
(2)②、③、⑤分别为O、Na、S元素,离子的电子层越多,离子半径越大,电子层相同时,离子的核电荷数越大,离子半径越小;
(3)元素④和⑥分别为硅和Cl,二者形成的化合物四氯化硅,四氯化硅为共价化合物,Si、Cl原子最外层都满足8电子稳定结构,据此写出四氯化硅的电子式.
解答 解:根据各元素在周期表中的相对位置可知,①为H元素、②为O元素、③为Na元素、④为Si元素、⑤为S元素、⑥为Cl元素,
(1)②为O元素,氧离子的核电荷数为8,核外电子总数为10,其离子结构示意图为: ,
,
故答案为: ;
;
(2)②、③、⑤分别为O、Na、S元素,离子的电子层越多,离子半径越大,则S2-的离子半径最大,电子层相同时,离子的核电荷数越大,离子半径越小,则离子半径:O2->Na+,所以离子半径大小为:S2->O2->Na+,
故答案为:S2->O2->Na+;
(3)元素④和⑥形成的化合物四氯化硅,四氯化硅为共价化合物,Si、Cl原子最外层都满足8电子稳定结构,其电子式为 ,
,
故答案为: .
.
点评 本题考查了位置、结构与性质的综合应用,题目难度不大,根据元素周期表结构正确推断元素为解答结构,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列关于实验原理或操作的叙述中,不正确的是( )
| A. | 纸层析实验中,须将滤纸上的试样点浸入展开剂中 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度不一定要比水大 | |
| C. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| D. | 分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
11.二战期间,有支侦查小分队去炸毁德国法西斯的一座隐蔽且戒备森严的军火工厂,结果他们用十多只涂有化学药剂的老鼠完成了任务.据你推测这种化学药剂可能是( )
| A. | TNT | B. | 白磷的CS2溶液 | C. | 黑火药和甘油 | D. | KMnO4和H2SO4 |
8.下列叙述不正确的是( )
| A. | 0.1mol Fe和0.1mol Zn被氧化,共转移电子0.2mol | |
| B. | 标准状况下,22.4L N2和N2O4的混合物,含N原子2mol | |
| C. | 16g O2和O3的混合物,含电子8mol | |
| D. | 常温常压下,12g CO和12g N2体积相等 |
3.如图药品和装置合理且能完成相应实验的是( )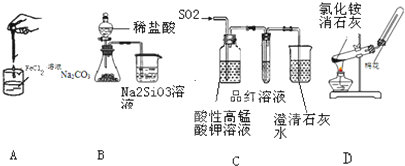

| A. | 制备氢氧化亚铁 | B. | 验证非金属性Cl>C>Si | ||
| C. | 检验二氧化硫中是否混有二氧化碳 | D. | 实验室制取并收集氨气 |
13.下列叙述中正确的是( )
| A. | 1 mol氢的质量是1 g | B. | 1 mol CO的质量为28 g•mol-1 | ||
| C. | 阿伏加德罗常数等于6.02×1023 | D. | 3.01×1023个SO2分子约是0.5 mol |
18.科学家合成了世界上最大的碳氢分子,其中一个分子由1134个碳原子和1146个氢原子构成,关于此物质说法错误的是( )
| A. | 是烃 | B. | 不能在空气中燃烧 | ||
| C. | 常温下呈固态 | D. | 可能发生加成反应 |

 .
. .
.